
| A、2:3 | B、4:3 |
| C、10:3 | D、11:3 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
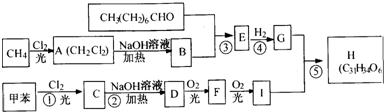
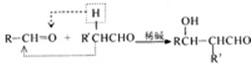
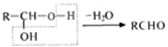 试回答:
试回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:

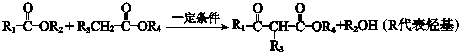
查看答案和解析>>
科目:高中化学 来源: 题型:
 2014年5月中美科学家研究发现,常温下氢气分子可以在碳纳米管内与水形成氢气水合物,其原理类似于可燃冰的形成,这项研究有望能洁净安全地储存氢气.下列说法正确的是( )
2014年5月中美科学家研究发现,常温下氢气分子可以在碳纳米管内与水形成氢气水合物,其原理类似于可燃冰的形成,这项研究有望能洁净安全地储存氢气.下列说法正确的是( )| A、碳纳米管以水合物储存氢气属化学变化 |
| B、碳纳米管与金刚石互为同素异形体 |
| C、氢气水合物与可燃冰是同一物质 |
| D、氢气与纳米管内的水分子形成共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
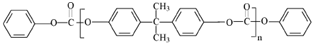 )的合成路线如图所示:
)的合成路线如图所示: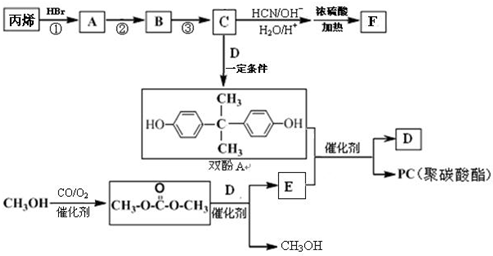
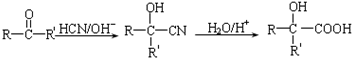
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com