
对溶液中的离子反应有下列说法,其中正确的是( )
①不可能是氧化还原反应 ②只能是复分解反应 ③有可能是置换反应 ④不可能有分子参加
A.①② B.只有③ C.②④ D.①④
科目:高中化学 来源: 题型:
 (2013?日照二模)CO、NO、NO2、SO2等都是污染大气的有害气体,对其进行回收利用是节能减排的重要课题.
(2013?日照二模)CO、NO、NO2、SO2等都是污染大气的有害气体,对其进行回收利用是节能减排的重要课题.c(N
| ||
| c(NH3?H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| NO | - 4 |
| 测试时间/h | 0 | 1 | 2 | 3 | 4 | 6 | 6 |
| 样本的Ph | 4.93 | 4.72 | 4.63 | 4.58 | 4.56 | 4.55 | 4.55 |

查看答案和解析>>
科目:高中化学 来源:2012-2013学年山东省日照市高三第二次模拟考试理综化学试卷(解析版) 题型:填空题
CO、NO、NO2、SO2等都是污染大气的有害气体,对其进行回收利用是节能减排的重要课题。
(1)上述四种气体直接排入空气中会引起酸雨的有 。
(2) 可用尿素
可用尿素 还原(尿素中C元素的化合价为+4价),反应的方程式为:
还原(尿素中C元素的化合价为+4价),反应的方程式为: 。当消耗掉12g尿素时,转移电子的物质的量是
。
。当消耗掉12g尿素时,转移电子的物质的量是
。
(3)SNCR-SCR是一种新型的烟气脱硝技术(除去烟气中的 ),改流程中发生的主要反应有:
),改流程中发生的主要反应有:

则反应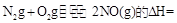 KJ/mol
KJ/mol
(4)CO可用于合成甲醇,反应方程式为 。在一容积可变的密闭容器中充有10mol CO和20molH2,在催化剂作用下发生反应生成甲醇,CO的平衡转化率(a)与温度(T)、压强(P)的关系如图所示。
。在一容积可变的密闭容器中充有10mol CO和20molH2,在催化剂作用下发生反应生成甲醇,CO的平衡转化率(a)与温度(T)、压强(P)的关系如图所示。
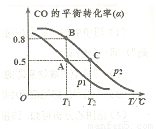
则该反应是 0(填“>”或“<”)。若达到平衡状态A时,容器的体积为10L,则在平衡状态B时容器的体积为 L。
0(填“>”或“<”)。若达到平衡状态A时,容器的体积为10L,则在平衡状态B时容器的体积为 L。
(5)工业上用氨水将来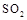 转化成都(NH4)2SO3,再氧化成(NH4)2SO4,(NH4)2SO4溶液中离子浓度大小顺序为
;已知25℃时,0.05mol/L(NH4)2SO4溶液的
转化成都(NH4)2SO3,再氧化成(NH4)2SO4,(NH4)2SO4溶液中离子浓度大小顺序为
;已知25℃时,0.05mol/L(NH4)2SO4溶液的 ,则
,则 =
(用含a的代数式表示,已知
=
(用含a的代数式表示,已知 的电离常数
的电离常数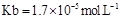 )。
)。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 离子的比例有呈明显上升的趋势.通过该地的雨水样本分析,推测该地的大气污染特征是______.
离子的比例有呈明显上升的趋势.通过该地的雨水样本分析,推测该地的大气污染特征是______.| 测试时间/h | 0 | 1 | 2 | 3 | 4 | 6 | 6 |
| 样本的Ph | 4.93 | 4.72 | 4.63 | 4.58 | 4.56 | 4.55 | 4.55 |

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
(08黄桥中学模拟)(8分)电荷相反的离子相互靠近时,由于相反电荷的相互作用,离子的电子云发生变化,称为极化。被异号离子极化而产生离子电子云变形的性质,称为该离子的变形性。阴阳离子都有极化作用和变形性两方面,但由于阳离子的半径小,电场集中,阴离子则相反,所以阳离子的极化作用较大,阴离子的变形性较大。一般说来,阳离子半径越小,电荷越高,极化作用越强;阴离子半径越大,负电荷越多,变形性越强。阴离子被极化后产生变形,正负电荷重心不重合,反过来又可对阳离子产生极化作用,称之为附加极化。附加极化的结果,使阴阳离子产生强烈变形,外层电子云发生重叠,键的极性减弱,键长变短,有离子键向共价键过渡,使物质的溶解度变小,热稳定性降低, 颜色加深…
含复杂阴离子的化合物中,复杂离子中的正态原子对负态原子有极化作用,化合物中的阳离子对阴离子中的负态原子也有极化作用,后一作用与前一作用方向相反,称之为反极化作用。反极化作用的存在表现为阳离子与阴离子中的正态原子共同整体争夺负性原子,使阴离子内部化学键削弱,易发生断键。
(1)BaCO3,FeCO3,ZnCO3,CaCO3分解温度由高到低的顺序是
(2)COF2,COBr2,COCl2,COI2颜色由浅到深的顺序是
(3)试解释Na2CO3的分解温度比NaHCO3高的原因。
(4)碳酸钠易溶于水,碳酸氢钠微溶于水,按理说向饱和的碳酸钠溶液中通入CO2气体应有晶体析出,流行试题就是依此编出来的,当你去做这个实验时,开始时向饱和的碳酸钠溶液中通入CO2气体却没有晶体析出为什么?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com