
【题目】氢能是极具发展潜力的清洁能源,氢气的开发和综合利用是目前全球重要的科研项目之一。回答下列问题:
(1)T℃时,向体积均为1L的甲、乙两个恒容容器中分别加入足量碳和0.1molH2O(g),发生反应:H2O(g)+C(s)CO(g)+H2(g) △H>0。甲容器控制绝热条件,乙容器控制恒温条件,两容器中压强随时间的变化如图所示。
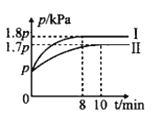
①图中代表甲容器的曲线为__(填“Ⅰ”或“Ⅱ”)。
②下列关于甲容器反应体系的说法错误的是__。
A.当水蒸气的体积分数不再发生变化,反应达到平衡状态
B.从密闭容器中分离出部分固体碳,H2的体积分数减小
C.缩小容器体积,平衡逆向移动,平衡常数减小
D.向平衡体系中充入少量水蒸气,再次平衡后,容器中c(CO)增大
③乙容器中,从反应开始到达平衡,v(H2O)=__molL-lmin-l;T℃下,该反应的平衡常数Kp=___(用含p的代数式表示)。
(2)对于反应aA(g)+bB(g)cC(g)+dD(g),速率方程v═kcm(A)cn(B),k为速率常数(只受温度影响),m+n为反应级数。已知H2(g)+CO2(g)CO(g)+H2O(g),CO的瞬时生成速率=kcm(H2)c(CO2)2。一定温度下,控制CO2起始浓度为0.25molL-1,改变H2起始浓度,进行以上反应的实验,得到CO的起始生成速率和H2起始浓度呈如图所示的直线关系。
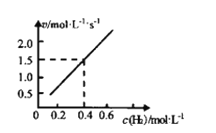
①该反应的反应级数为__。
②速率常数k=__。
③当H2的起始浓度为0.2molL-1,反应进行到某一时刻时,测得CO2的浓度为0.2molL-1,此时CO的生成瞬时速率v=__molL-ls-1。
【答案】Ⅱ BD 0.01 3.2p 3 60 0.5625
【解析】
(1)①该反应为吸热反应,甲容器绝热条件下体系温度降低,反应速率低,达平衡所需时间长,平衡逆向移动,体系压强降低;
②A.水蒸气体积分数不变,即各物质浓度不变;
B.固体无浓度,不改变平衡移动;
C.缩小容器体积,压强增大,平衡逆移,绝热情况下体系温度升高,平衡常数减小;
D.向平衡体系中充入少量水蒸气,根据勒夏特列原理分析;
③列三段式:
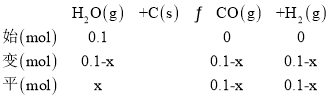
压强与物质的量成正比,![]() ,解出x,根据v(H2O)=
,解出x,根据v(H2O)=![]() =
=![]() 进行计算,平衡常数K=
进行计算,平衡常数K=![]() ;
;
(2)①根据N2的瞬时生成速率v=kcm(H2)c2(CO2)与H2起始浓度呈直线关系进行分析;
②将图象上的点(0.4,1.5)代入瞬时速率中即可得结果;
③由于CO2起始浓度为0.25molL-1,反应进行到某一时刻时,测得CO2的浓度为0.2molL-1,△c(CO2)=(0.25-0.2)mol/L=0.05mol/L,△c(H2)=△c(CO2)=0.05mol/L,结合瞬时速率公式进行计算。
(1)①甲容器控制绝热条件,该反应吸热,体系温度低,转化率低,产生气体总量少,压强较小,则图中代表恒容绝热密闭容器的曲线为Ⅱ;
②A.该反应前后气体体积不相等,当水蒸气的体积分数不再发生变化时,反应达到平衡状态,故A正确;
B.碳是固体,平衡时从密闭容器中分离出部分固体碳,不影响平衡体系,各气体的体积分数不变,故B错误
C.甲容器控制绝热条件,该反应吸热,压缩体积,压强增大,体系温度升高,平衡逆向移动,平衡常平衡常数减小,故C正确;
D.向平衡体系中充入少量水蒸气,根据勒夏特列原理知容器中c(CO)降低,故D错误;
答案选BD;
③乙容器为恒温恒容密闭容器,曲线Ⅰ代表该容器的变化,设平衡时水蒸气的物质的量为x,8min达到平衡,压强变为原来的1.8倍,列三段式:
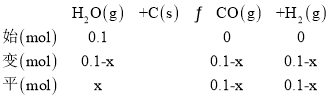
![]() ,解得x=0.02,v(H2O)=
,解得x=0.02,v(H2O)=![]() =0.01 molL-1min-1;该反应的平衡常数Kp=
=0.01 molL-1min-1;该反应的平衡常数Kp=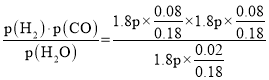 =3.2p。
=3.2p。
(2)①根据CO的瞬时生成速率v=kcm(H2)c2(CO2)与H2起始浓度呈直线关系可知,m=1,该反应的反应级数为1+2=3;
②将图象上的点(0.4,1.5)代入v=kc(H2)c2(CO2)中有:1.5=0.4×k×0.252,即k=60;
③由于CO2起始浓度为0.25molL-1,反应进行到某一时刻时,测得CO2的浓度为0.2molL-1,△c(CO2)=(0.25-0.2)mol/L=0.05mol/L,△c(H2)=△c(CO2)=0.05mol/L,H2的瞬时浓度为c(H2)=(0.2-0.05)mol/L=0.15mol/L,此时CO的生成瞬时速率v=60×0.15×0.252=0.5625。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:
【题目】BMO(Bi2MoO6)是一种高效光催化剂,可用于光催化降解苯酚,原理如图所示。下列说法正确的是( )
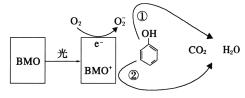
A.该过程的总反应:C6H6O+7O2![]() 6CO2+3H2O
6CO2+3H2O
B.该过程中BMO表现出较强氧化性
C.光催化降解过程中,光能转化为化学能、电能等
D.①和②中被降解的苯酚的物质的量之比为3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向10 mL 0.1 mol/L CuCl2溶液中滴加0.1 mol/L的Na2S溶液,滴加过程中溶液中-lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示,下列有关说法不正确的是
(已知:Ksp(ZnS)=3×10-25mol2/L2)

A.a、b、c三点中,水的电离程度最大的为b点
B.Na2S溶液中:2c(S2-)+2c(HS-)+2c(H2S)=c(Na+)
C.该温度下Ksp(CuS)=10-35.4 mol2/L2
D.向100 mL Zn2+、Cu2+浓度均为10-5 mol/L的混合溶液中逐滴加入10-4 mol/L的Na2S溶液,Cu2+先沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置中所用仪器、试剂、现象和结论均正确的是
选项 | 装置 | 现象 | 结论 |
A |
| 装置Ⅲ中有浅黄色沉淀生成 | 苯和浓溴水发生取代反应 |
B |
| 高锰酸钾溶液褪色,溴的四氯化碳溶液褪色 | 石蜡油的分解产物中含有乙烯 |
C |
| 分液漏斗液体流下,锥形瓶中产生大量气体 | 快速制备和收集一定量的氨气 |
D |
| 试管中依次出现白色,黄色沉淀 | 说明 Ksp(AgCl)>Ksp(AgI) |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,分别用 0.01mol/L 的 NaOH 溶液滴定与之等浓度的体积均为 25.00mL 的 HA、H3B(三元酸)溶液,溶液的 pH 随V(NaOH)变化曲线如图所示,下列说法错误的是
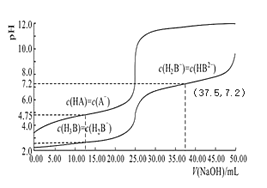
A.常温下 K(HA)数量级约为10-5
B.常温下 0.01mol/L 的 NaH2B溶液的 pH 大于 7
C.NaOH 溶液滴定 HA 溶液应选择酚酞作为指示剂
D.当横坐标为 37.50时,溶液中存在:2c(H+)+c(H2B-)+3c(H3B)=2c(OH-)+3c(B3-)+c(HB2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.某温度时 N2(g)+3H2(g)![]() 2NH3(g),正、逆反应的平衡常数分别为 K1、K2,则 K1·K2=1
2NH3(g),正、逆反应的平衡常数分别为 K1、K2,则 K1·K2=1
B.若一个可逆反应的化学平衡常数很大,则该反应会在较短的时间内完成
C.氢氧燃料电池是一种将热能转化为电能的装置
D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酒精检测仪可帮助执法交警测试驾驶员饮酒的多少,其工作原理示意图如下图所示。反应原理为:CH3CH2OH+O2=CH3COOH+H2O,被测者呼出气体中所含的酒精被输送到电池中反应产生微小电流,该电流经电子放大器放大后在液晶显示屏上显示其酒精含量。下列说法正确的是( )
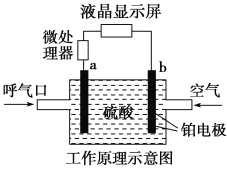
A.电解质溶液中的H+移向a电极
B.b为正极,电极反应式为:O2+4H++4e-=2H2O
C.若有0.4 mol电子转移,则在标准状况下消耗4.48 L氧气
D.呼出气体中酒精含量越高,微处理器中通过的电流越小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是
A.2.8g14N2与14C16O的混合物中,中子数目为 l.4NA
B.含 0. l molFeCl3的溶液与0. l mol 锌充分反应,转移电子数为0.l NA
C.标准状况下,5.6gC4H8中 C-C 的数目可能为0.4NA
D.某温度下,1LpH=9 的 Na2CO3 溶液中,水电离产生的OH-数目为10-5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1 g氢气完全燃烧生成水蒸气时放出热量121 kJ,且氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1mol H-O键形成时放出热量463 kJ,则氢气中1mol H-H键断裂时吸收热量为
A.920 kJB.557 kJC.436 kJD.188 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com