
甲烷中混有乙烯,欲除乙烯得到纯净的甲烷,可依次将其通过下列哪组试剂的洗气瓶( )
A.澄清石灰水,浓H2SO4 B.溴水,浓H2SO4
C.酸性高锰酸钾溶液,浓H2SO4 D.浓H2SO4,酸性高锰酸钾溶液
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
某同学用沉淀法测定Na2CO3和NaOH混合物中NaOH的质量分数,有关叙述如下。①可以使用MgCl2溶液作沉淀剂,使OH-转化为氢氧化镁沉淀 ②检验CO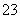 是否完全沉淀的操作方法是取上层清液,向其中继续滴加沉淀剂溶液,观察是否有沉淀继续生成 ③用BaCl2溶液代替CaCl2溶液作沉淀剂,优点是能提高实验结果的准确度 ④用BaCl2溶液代替CaCl2溶液作沉淀剂,优点是CO
是否完全沉淀的操作方法是取上层清液,向其中继续滴加沉淀剂溶液,观察是否有沉淀继续生成 ③用BaCl2溶液代替CaCl2溶液作沉淀剂,优点是能提高实验结果的准确度 ④用BaCl2溶液代替CaCl2溶液作沉淀剂,优点是CO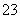 能100%转化为沉淀。其中正确的叙述是( )
能100%转化为沉淀。其中正确的叙述是( )
A.①② B.②③ C.①③④ D.都正确
查看答案和解析>>
科目:高中化学 来源: 题型:
将1.00 mol二氧化硫和1.00 mol氧气通入1.00 L的密闭容器中,分别在500 K,600 K,700 K三个不同的温度下进行2SO2+O2 2SO3反应,反应过程中SO3浓度随时间的变化如下面表格所示:
2SO3反应,反应过程中SO3浓度随时间的变化如下面表格所示:
表一:500 K
| 时间(min) | 0 | 5 | 10 | 15 | 20 | 25 |
| SO3浓度(mol·L-1) | 0 | 0.10 | 0.15 | 0.20 | 0.25 | 0.30 |
| 时间 | 30 | 35 | 40 | 45 | 50 | 55 |
| SO3浓度(mol·L-1) | 0.35 | 0.40 | 0.50 | 0.55 | 0.60 | 0.60 |
表二:600 K
| 时间(min) | 0 | 5 | 10 | 15 | 20 | 25 |
| SO3浓度(mol·L-1) | 0 | 0.20 | 0.30 | 0.40 | 0.50 | 0.50 |
表三:700 K
| 时间(min) | 0 | 5 | 10 | 15 | 20 | 25 |
| SO3浓度(mol·L-1) | 0 | 0.25 | 0.35 | 0.35 | 0.35 | 0.35 |
(1)从上面三个表的数据可以判断该反应是__________反应(填“吸热”或“放热”),利用表一计算0~40 min内用SO2表示该反应的化学反应速率v(SO2)=__________mol·L-1·min-1。
(2)对该反应,下面的说法正确的是__________。
A.当容器中的压强不再变化时,该反应就达到平衡
B.达到平衡时v正(SO2)=v逆(SO3)
C.平衡时c(SO2)=c(SO3)
D.当由500 K平衡状态时升高温度至600 K时,重新达到平衡状态时,容器的压强减小
(3)从上面三个表的数据,温度对该反应的反应速率和平衡移动的影响是_____________________________________________________________________。
(4)计算在600 K时的平衡常数(写出计算过程,最后结果取两位有效数字)。
(5)下图曲线(Ⅰ)是在500 K时SO3浓度的变化曲线,请你在图中画出在550 K进行上述反应的曲线,并标明曲线(Ⅱ)。
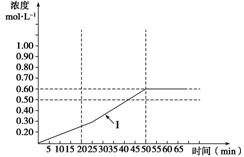
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于蛋白质的叙述正确的是 ( )
A.天然蛋白质的组成元素只有磷、氢、氧、氮
B.加热会使蛋白质变性,因此食生鸡蛋的营养价值更高
C.向鸡蛋中加食盐,会使蛋白质凝固变性
D.用一束光照射蛋白质溶液,可以产生丁达尔现象
查看答案和解析>>
科目:高中化学 来源: 题型:
糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质。以下叙述正确的是 ( )
A.植物油不能发生水解反应 B.淀粉水解的最终产物是葡萄糖
C.葡萄糖能发生氧化反应和水解反应 D.蛋白质水解的产物为纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家近年来研制出一种新型细菌燃料电池,利用细菌将有机物转化为氢气,氢气进入以硫酸为电解质的燃料电池发电。电池负极反应为 ( )
A H2+2OH--2e-=2H2O B O2+4H++4e-=2H2O
C H2-2e-=2H+ D O2+2H2O+4e-=4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应:2NO2(g) 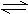 2NO(g)+O2(g)在体积固定的密闭容器中进行,能判断达到平衡状态的标志的是( )
2NO(g)+O2(g)在体积固定的密闭容器中进行,能判断达到平衡状态的标志的是( )
①单位时间内生成n mol O2的同时生成2n mol NO2
②生成O2的速率等于生成NO2的速率
③用NO2、NO、O2表示的反应速率的比为2∶2∶1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
A.①④⑥⑦ B .②③⑤ C.①③④⑤ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
在标准状况下,将a L NH3完全溶于水得到V mL氨水,溶液的密度为ρ g/cm3,溶质的质量分数为w,溶质的物质的量浓度为c mol/L。下列叙述中正确的是( )
①w=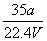 ×100% ②c=
×100% ②c=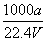
③向上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5 w
④向上述溶液中再加入1.5V mL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为c(Cl-)>c(NH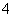 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
A.①③ B.②③ C.②④ D.①④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com