
| A、CsOH在水溶液中的电离方程式为CsOH═Ca++OH- | B、CsOH溶液能使酚酞试液变红 | C、因为CsCl是易溶于水的盐,所以CsOH溶液与稀盐酸不发生复分解反应 | D、CsOH溶液与MgCl2溶液发生复分解反应,有氢氧化镁沉淀生成 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
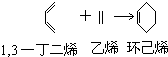
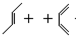 →
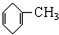
→
查看答案和解析>>
科目:高中化学 来源: 题型:
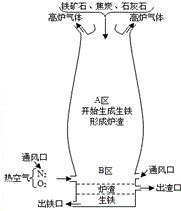 钢铁工业是国家工业的基础.下图是炼铁高炉及炉内化学变化过程示意图,根据图示回答下列问题.若图中采用的铁矿石的主要成分为氧化铁,请写出A区和B区所发生主要反应的化学方程式.
钢铁工业是国家工业的基础.下图是炼铁高炉及炉内化学变化过程示意图,根据图示回答下列问题.若图中采用的铁矿石的主要成分为氧化铁,请写出A区和B区所发生主要反应的化学方程式.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、主族金属单质与酸溶液反应置换出氢气的能力一定比过渡金属单质强 | B、第二周期元素的原子形成的阴离子半径随核电荷数的增大而增大 | C、同周期主族元素的原子形成简单离子的电子层结构相同 | D、元素原子的最外层电子数的多少与其非金属性的强弱无必然联系 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾既可以除去水中的悬浮物,也可以杀菌消毒 | B、可以通过电解明矾溶液来制取Al | C、用酒精灯加热铝箔至熔化,铝并不滴落,说明氧化铝的熔点比铝高 | D、可以用在某溶液中加入盐酸酸化的氯化钡溶液的方法来确定该溶液中是否含有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、小苏打可与酸反应,可用作治疗胃酸过多的药剂 | B、氯化铝是电解质,可电解其水溶液获得金属铝 | C、SO2具有漂白性,可用于将银耳漂白为“雪耳” | D、二氧化硅具有导电性,可用于生产光导纤维 |
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市高三第一次月考理综化学试卷(解析版) 题型:填空题
(16分)已知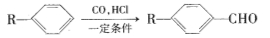
为合成某种液晶材料的中间体M,有人提出如下不同的合成路径:
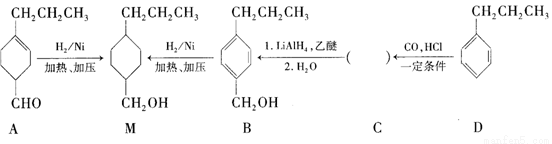
(1)常温下,下列物质能与A发生反应的有________(填序号)。
a.苯 b.Br2/CCl4c.乙酸乙酯d.KMnO4/H+溶液
(2)M中官能团的名称是_______,由C→B的反应类型为__________。
(3)由A催化加氢生成M的过程中,可能有中间产物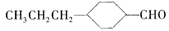 和______(写结构简式)生成。
和______(写结构简式)生成。
(4)检验B中是否含有C可选用的试剂是___________(任写一种名称)。
(5)物质B也可以由C10H13Cl与NaOH水溶液共热生成,C10H13Cl的结构简式为_______。
(6)C的一种同分异构体E具有如下特点:
a.分子中含—OCH2CH3 b.苯环上只有两种化学环境不同的氢原子
写出E在一定条件下发生加聚反应的化学方程式:____________。
查看答案和解析>>
科目:高中化学 来源:2015届广东省惠州市高三第二次调研考试化学试卷(解析版) 题型:选择题
下列陈述Ⅰ、Ⅱ正确并有因果关系的是
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | 氢氟酸具有酸性 | 氢氟酸可用于雕刻玻璃 |
B | SO2有氧化性 | SO2可用于漂白纸浆 |
C | NH3极易溶于水 | NH3可用作制冷剂 |
D | ClO2具有强氧化性 | ClO2可用于自来水的杀菌消毒 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com