
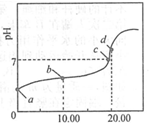
 �����£���0.01mol•L-1NaOH��Һ�ζ�20.00mL0.01mol•L-1CH3COOH��Һ�����õζ�������ͼ������˵����ȷ���ǣ�������
�����£���0.01mol•L-1NaOH��Һ�ζ�20.00mL0.01mol•L-1CH3COOH��Һ�����õζ�������ͼ������˵����ȷ���ǣ�������| A�� | a��PH=2 | |
| B�� | b���Ӧ����Һ�У�c��OH-��+c��CH3COO-��=c��Na+��+c��H+�� | |
| C�� | c���ʾNaOH��Һ��CH3COOH��Һǡ����ȫ��Ӧ | |
| D�� | d����õ���Һ�У�ˮ�ĵ���̶�С��ͬ���´�ˮ�ĵ���̶� |
���� A������Ϊ���ᣬ������ȫ���룻
B��b��ʱ��Һ�����ԣ���ϵ���غ���
C��c��ʱ��Һ�����ԣ���������������ǡ����ȫ��Ӧ������ҺӦ�ʼ��ԣ�
D��d��ʱ��Һ�ʼ��ԣ������ǡ���кͣ������ɴ����ƴٽ�ˮ�ĵ��룮
��� �⣺A������Ϊ���ᣬ������ȫ���룬��0.01mol•L-1 CH3COOH��ҺpH��2����A����
B����Һ�д��ڵ���غ㣺c��Na+��+c��H+��=c��OH-��+c��CH3COO-������B��ȷ��
C��������������Ʒ�Ӧ���ɴ����ƣ���������ǿ����������ˮ��Һ�ʼ��ԣ������ǡ�÷�Ӧʱ��ҺӦ�óʼ��ԣ���C����Һ�����ԣ�˵�����������C����
D��d��ʱ��Һ�ʼ��ԣ�����ǡ���кͣ���ȫ��Ӧ���ɴ����ƣ�ˮ��ʼ��ԣ��ٽ�ˮ�ĵ��룬��d��ˮ�ĵ���̶ȴ���ͬ���´�ˮ�ĵ���̶ȣ���D����
��ѡB��
���� ������NaOH�ζ�CH3COOH�ĵζ�����Ϊ���壬���������ˮ�⡢��Һ����Ũ�ȵĴ�С�Ƚϵȣ��Ѷ��еȣ�ע������Ũ�ȴ�С�Ƚ��е���غ㣬����Ӱ��������ʵĵ��������ˮ������أ�ע����ػ���֪ʶ�Ļ��ۣ��ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{1-a}{7}$ | B�� | $\frac{3}{4}$a | C�� | $\frac{6}{7}$��1-a�� | D�� | $\frac{12}{13}$��1-a�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ѹ������ﵽ��ƽ��ʱ��CO��Ũ������ı�����CO2��Ũ������ı������� | |
| B�� | ���ʹ�ϵ��2v��CO2��=v��CO�� | |
| C�� | ת�Ƶ��������¶����߶����� | |
| D�� | �����ܶ����Ž�̿�����Ӷ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C4H9OH | B�� | C6H5CH2OH | C�� | C6H5OH | D�� | 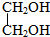 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
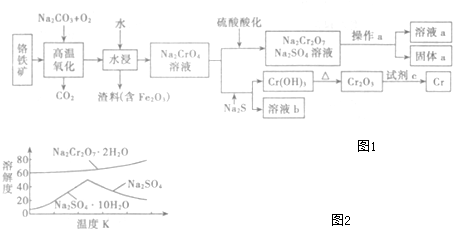
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| R | Q | ||
| M | T |
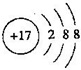 �� Ԫ��M��Ԫ�����ڱ��е�λ���ǵ������ڵ�VIA�壮
�� Ԫ��M��Ԫ�����ڱ��е�λ���ǵ������ڵ�VIA�壮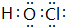 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ȫ�� | B�� | �ڢۢܢݢ� | C�� | �ܢݢ� | D�� | �ݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
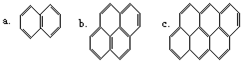 ������������к��г���������������һЩ�ɷֿ���Ϊ��ͬϵ����磺�Դ�˳���Ʋ������d��e��f���ȣ��ڸ�ϵ�л������У�̼�����ٷֺ����ǣ�������
������������к��г���������������һЩ�ɷֿ���Ϊ��ͬϵ����磺�Դ�˳���Ʋ������d��e��f���ȣ��ڸ�ϵ�л������У�̼�����ٷֺ����ǣ�������| A�� | 100% | B�� | 56% | C�� | 97.3% | D�� | 93.8% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
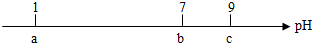
| A�� | �����£�0.1mol•L-1��HCl��Һ��pH=1 | |
| B�� | ��pH=7ʱ������NH3•H2O��Һ���������10mL | |
| C�� | ��7��pH��9ʱ����Һ��c��NH4+����c��Cl-�� | |
| D�� | �����μ�0.1mol•L-1��NH3•H2O��Һ����Һ��pH���տ��Ա仯��13 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com