
含有SiO2杂质的赤铁矿粉末10 g和50 mL H2SO4溶液充分充分反应后,再加入5.04 g铁粉,这时能产生氢气448 mL(标况),反应后余铁粉1.12 g。
计算 :(1)赤铁矿中铁的质量分数(2)H2SO4的物质的量浓度
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| ||

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的通常有两种工艺。因向铝土矿中加入NaOH时形成的赤泥(残渣)中常含有铝硅酸钠,故流程乙常处理SiO2含量小于8%的铝土矿,若SiO2含量较高则可采用流程甲来处理。

请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的离子方程式为 。
(2)流程乙加入烧碱后生成SiO32-的离子方程式为 。
(3)流程甲滤液D中通入过量CO2的化学方程式为 。
(4)“通入过量CO2”能否改用盐酸 ,原因是 。
(5)滤液E、K中溶质的主要成分是 (填化学式),写出该溶质的一种用途________。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年浙江省余姚中学高一上学期期中化学(理)试卷(化学实验班) 题型:填空题
从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的通常有两种工艺。因向铝土矿中加入NaOH时形成的赤泥(残渣)中常含有铝硅酸钠,故流程乙常处理SiO2含量小于8%的铝土矿,若SiO2含量较高则可采用流程甲来处理。
请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的离子方程式为 。
(2)流程乙加入烧碱后生成SiO32-的离子方程式为 。
(3)流程甲滤液D中通入过量CO2的化学方程式为 。
(4)“通入过量CO2”能否改用盐酸 ,原因是 。
(5)滤液E、K中溶质的主要成分是 (填化学式),写出该溶质的一种用途________。
查看答案和解析>>
科目:高中化学 来源:2014届浙江省高一上学期期中化学(理)试卷(化学实验班) 题型:填空题
从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的通常有两种工艺。因向铝土矿中加入NaOH时形成的赤泥(残渣)中常含有铝硅酸钠,故流程乙常处理SiO2含量小于8%的铝土矿,若SiO2含量较高则可采用流程甲来处理。
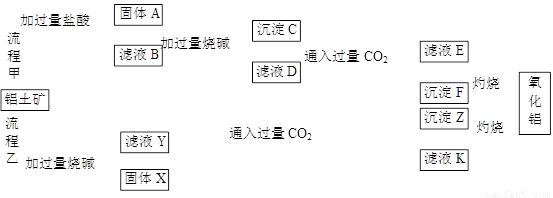
请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的离子方程式为 。
(2)流程乙加入烧碱后生成SiO32-的离子方程式为 。
(3)流程甲滤液D中通入过量CO2的化学方程式为 。
(4)“通入过量CO2”能否改用盐酸 ,原因是 。
(5)滤液E、K中溶质的主要成分是 (填化学式),写出该溶质的一种用途________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com