
设NA表示阿伏加德罗常数,下列叙述中正确的是
A.常温常压下,11.2 LNH3所含的原子数为2NA
B.常温常压下,80 g SO3含有的氧原子数为3NA
C.标准状况下,22?4 L H2中所含原子数为NA
D.一定条件下,56g铁粉与足量的Cl2完全反应转移电子数目为2NA
科目:高中化学 来源:2013-2014江苏省海门市第一学期期末教学质量调研高一化学试卷(解析版) 题型:填空题
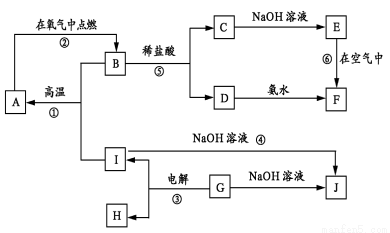
(12分)下图表示各物质之间的转化关系。已知:常温下B、D、F、G、I、J是气体, F、G是空气中的主要成分,D是一种碱性气体。A中阴、阳离子个数比是1∶1, E是一种黑色氧化物,H是紫红色金属单质。(部分生成物和反应条件省略)
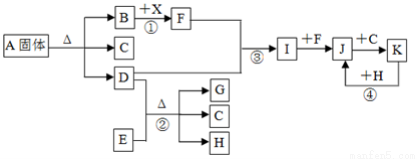
请按要求填空:
(1)A物质的化学式是 ;
(2)反应③的化学方程式是 ;
反应④的离子方程式是 ;
(3)反应①中产生标准状况下1.12L气体F,则转移的电子数目是 ;
(4)检验溶液A中阳离子的方法是
;
(5)反应②中氧化剂是 ;
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省无锡市高一下学期期末考试化学试卷(解析版) 题型:简答题
酯类是工业上重要的有机原料,具有广泛用途。
乙酸苯甲酯( )对花香和果香的香韵具有提升作用,故常用于化妆品和食品工业。乙酸苯甲酯的合成路线如下:
)对花香和果香的香韵具有提升作用,故常用于化妆品和食品工业。乙酸苯甲酯的合成路线如下:


(1)B中含氧官能团的名称是 ;
反应③的类型是 ,①的化学方程式是 。
(2)下列物质中能与A的水溶液反应的是 。
a.CaCO3 b.NaOH c.CuSO4 d.NaCl
(3)下列物质中与甲苯互为同系物的是 。
a.  b.
b. c.
c. d.
d.
(4)绿色化学的核心内容之一是“原子经济性”,即原子的理论利用率为100%。下列转化符合绿色化学要求的是_____(填序号)。
a.乙醇制取乙醛 b.甲苯制备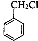 c.2CH3CHO+O2
c.2CH3CHO+O2 2A
2A
(5)苯甲酸苯甲酯可用作香料、食品添加剂及一些香料的溶剂,还可用作塑料、涂料的增
塑剂。工业上常用苯甲酸钠与氯甲基苯( ))在催化剂作用下反应制备。
))在催化剂作用下反应制备。
已知:
流程图示例如下:
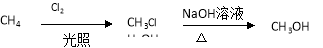
设计以甲苯为原料(无机试剂任选)合成苯甲酸苯甲酯的流程图 。
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省无锡市高一下学期期末考试化学试卷(解析版) 题型:选择题
下列说法中正确的是
A. 、
、 、
、 互为同素异形体
互为同素异形体
B.O2与O3互为同位素
C.CH3-CH2-OH与CH3-O-CH3互为同分异构体
D.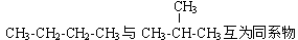
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省高一期末模拟化学试卷(解析版) 题型:推断题
(12分) A-I分别表示中学化学中的常见物质,它们之间的相互转化关系如下图所示(部分反应物、生成物没有列出),且已知G是一种两性氧化物,A、B、C、D、E、F六种物质中均含有同一种元素,F为红褐色沉淀。
请填写下列空白:
(1) A、B、C、D、E、F六种物质中所含的同一种元素是 (写元素符号)。
(2) 写出物质C、G的化学式:C ,G 。
(3) 写出反应①、④的化学方程式:反应①: 。反应④: 。
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省高一期末模拟化学试卷(解析版) 题型:选择题
已知浓H2SO4和Fe3+都可以将Cu氧化(Fe3+与Cu的反应为:2Fe3+ + Cu = 2Fe2+ + Cu2+),浓H2SO4还可以将Br-氧化成Br2,Fe与Br2反应生成FeBr3,则有关物质氧化性强弱的顺序为
A.H2SO4(浓) > Cu2+ > Fe3+ > Br2 B.H2SO4(浓) > Br2 > Fe3+ > Cu2+
C.Br2 > H2SO4(浓) > Cu2+ > Fe3+ D.Cu2+ > Fe3+ > Br2 > H2SO4(浓)
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省高二下学期阶段测试5月 化学试卷(解析版) 题型:简答题
(12分) (1)已知:蒸发1 mol Br2(l)需要吸收的能量为 30 kJ,其他相关数据如下表:
物质 | H2(g) | Br2(g) | HBr(g) |
1 mol分子中化学键断裂时需要吸收的能量/kJ | 436 | 200 | 369 |
H2(g)+Br2(l)=2HBr(g) ΔH= 。
(2)常温下,将pH均为2的氢溴酸、乳酸(α—羟基丙酸)稀释100倍后,有一种酸的pH=4。请写出乳酸钠溶液中的水解离子方程式: 。
(3)常温下,用0.100 0 mol·L-1 NaOH溶液分别滴定20.00 mL 0.100 0 mol·L-1 HBr溶液和20.00 mL0.100 0 mol·L-1 CH3COOH溶液,得到2条滴定曲线,如图所示:
①根据图1和图2判断,滴定HBr溶液的曲线是 (填“图1”或“图2”);
②a= mL;
③c(Na+)=c(CH3COO-)的点是 点;
④E点对应溶液中离子浓度由大到小的顺序为 。
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省高二下学期阶段测试5月 化学试卷(解析版) 题型:选择题
下列叙述中,正确的是
A.在一个基态多电子的原子中,可以有两个运动状态完全相同的电子
B.在一个基态多电子的原子中,不可能有两个能量完全相同的电子
C.如果某一基态原子3p轨道上仅有2个电子,它们自旋方向必然相反
D.在一个基态多电子的原子中,M层上的电子能量肯定比L层上的电子能量高
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省徐州市高三考前模拟化学试卷(解析版) 题型:选择题
下列有关物质性质的应用错误的是
A.H2O2溶液有氧化性,可用于杀菌消毒
B.氯化镁是一种电解质,可用于电解法制镁
C.液氨汽化时要吸收大量的热,可用作制冷剂
D.Na2SO4能使蛋白质发生变性,可用于提纯蛋白质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com