
| A. | 氢氧化钠的摩尔质量是40 g | |
| B. | 1 mol NaOH的质量是40 g/mol | |
| C. | 1gH2和lgN2含分子数相等 | |
| D. | 等质量的N2、CH4、CO、H2O中,CH4含分子数最多 |
分析 A、摩尔质量的单位是g/mol;
B、质量的单位是g;
C、摩尔质量越大,分子数越小;
D、摩尔质量越小,分子数越多.
解答 解:A、摩尔质量的单位是g/mol,所以氢氧化钠的摩尔质量是40 g/mol,故A错误;
B、质量的单位是g,所以1 mol NaOH的质量是40 g,故B错误;
C、摩尔质量越大,分子数越小,氢气和氮气的摩尔质量不等,所以等质量的两种混合气体的分子数不等,故C错误;
D、摩尔质量越小,分子数越多,而在N2、CH4、CO、H2O中甲烷的摩尔质量最小,所以等质量的N2、CH4、CO、H2O中,CH4含分子数最多,故D正确;
故选D.
点评 本题考查物质的量有关计算,难度不大,注意对公式的理解与灵活应用.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-242KJ•mol-1(燃烧热) | |
| B. | 2NaOH(aq)+H2SO4(aq)═Na2SO4(aq)+2H2O(l)△H=-114KJ•mol-1(中和热) | |
| C. | H2O(l)═H2(g)+$\frac{1}{2}$O2(g)△H=-286KJ•mol-1(反应热) | |
| D. | C(石墨,S)+$\frac{1}{2}$O2(g)═CO(g)△H=-111KJ•mol-1(反应热) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ③②① | C. | ②③① | D. | ①③② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2gH2中含有的分子数为NA | |
| B. | 1mol Zn变成Zn2+时失去的电子数为NA | |
| C. | 1L1mol•L-1MgCl2溶液中含有的Cl-数为NA | |
| D. | 常温常压下,22.4LO2含有的原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl3溶液使蓝色石蕊试纸变红:Fe3++3H2O═3H++Fe(OH)3 | |
| B. | FeCl3溶液中滴加氨水出现红褐色沉淀:Fe3++3OH-═Fe(OH)3↓ | |
| C. | 用FeCl3溶液腐蚀印刷电路板:Fe3++Cu═Cu2++Fe2+ | |
| D. | 检验溶液中的Fe3+用KSCN溶液:Fe3++3SCN-?Fe(SCN)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
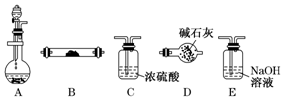 如图是用于气体制备、干燥、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去).请根据下列要求回答问题.
如图是用于气体制备、干燥、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去).请根据下列要求回答问题.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
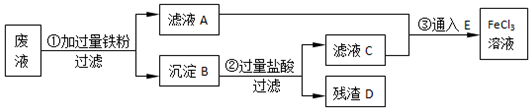
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有NA个氦原子的氦气在标准状况下的体积约为11.2L | |
| B. | 在常温常压下,46g NO2和N2O4混合气体所含氧原子数目为2NA | |
| C. | 将1L 2mol/L的FeCl3溶液制成胶体后,其中含有氢氧化铁胶粒数为2NA | |
| D. | 标准状况下,11.2LCCl4含有的分子数为0.5NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com