
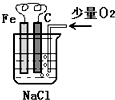
 分析图,按要求写出有关反应方程式:
分析图,按要求写出有关反应方程式:分析 由碳棒、铁片和氯化钠溶液组成的原电池中,Fe为负极,负极上Fe失电子生成亚铁离子,碳棒为正极,氧气在正极上得电子生成氢氧根离子,亚铁离子与氢氧根离子结合生成氢氧化亚铁,氢氧化亚铁被氧气氧化生成氢氧化铁,据此分析.
解答 解:(1)由碳棒、铁片和氯化钠溶液组成的原电池中,Fe为负极,负极上Fe失电子生成亚铁离子,碳棒为正极,氧气在正极上得电子生成氢氧根离子,碳棒上的电极反应式为:2H2O+O2+4e-═4OH-;
故答案为:2H2O+O2+4e-═4OH-;
(2)溶液中亚铁离子与氢氧根离子结合生成氢氧化亚铁,氢氧化亚铁被氧气氧化生成氢氧化铁,则溶液中发生的反应为2Fe+2H2O+O2═2Fe(OH)2,4Fe(OH)2+O2+2H2O=4Fe(OH)3;
故答案为:2Fe+2H2O+O2═2Fe(OH)2,4Fe(OH)2+O2+2H2O=4Fe(OH)3.
点评 本题考查了金属的电化学腐蚀及原电池原理,明确钢铁所处环境的酸碱性即可确定其电化学腐蚀类型,题目难度不大,注意把握电极方程式的书写方法.


科目:高中化学 来源: 题型:选择题

| A. | a、b、c的简单离子中,a的离子半径最大 | |
| B. | c、d、f最高价氧化物对应的水化物两两之间均可发生反应 | |
| C. | e的氢化物比f的氢化物的稳定性高 | |
| D. | a、e可形成一种新型无机非金属材料--高温结构陶瓷 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,32 g O2含有氧原子数为NA | |
| B. | 标准状况下,22.4 L H2O含有的分子数为NA | |
| C. | 18g H2O中含有的电子数为10NA | |
| D. | 0.5mol•L-1CaCl2溶液中含Cl-数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同条件下,电离平衡常数越小,表示弱电解质的电离能力越弱 | |
| B. | 相同条件下,化学平衡常数越大,表示该反应的反应速率越大 | |
| C. | 其它条件不变时,升高温度,化学平衡常数一定增大 | |
| D. | 多元弱酸各步电离平衡常数相互关系为K1<K2<K3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用过滤法除去Na2SO4溶液中的泥沙 | B. | 用蒸馏法分离溶液中的KCl和KNO3 | ||
| C. | 用萃取法将碘水中的I2萃取出来 | D. | 用蒸发法从NaCl溶液中得到NaCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com