
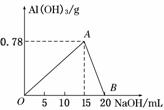
 向20 mL某物质的量浓度的AlCl3溶液中滴入2 mol/L NaOH溶液时,得到的Al(OH)3沉淀的质量与所滴加NaOH溶液的体积(mL)关系如图所示,试回答下列问题:
向20 mL某物质的量浓度的AlCl3溶液中滴入2 mol/L NaOH溶液时,得到的Al(OH)3沉淀的质量与所滴加NaOH溶液的体积(mL)关系如图所示,试回答下列问题:
(1)图中A点表示的意义是____________________。
(2)图中B点表示的意义是_______________________。
(3)上述两步用总的离子方程式可表示为:________________________________。
(4)假定反应混合物中有Al(OH)3沉淀0.39 g,则此时用去NaOH溶液的体积为________。
解析:把NaOH溶液滴入AlCl3溶液,先产生Al(OH)3沉淀,其质量最大值为A点,然后全部溶解消失(B点)。其总反应的离子方程式为:Al3++4OH-===AlO +2H2O。有0.39 g Al(OH)3沉淀生成,①当AlCl3过量时,加入NaOH使Al3+部分产生沉淀为0.39 g,通过Al3++3OH-===Al(OH)3↓可知用NaOH 7.5 mL。
+2H2O。有0.39 g Al(OH)3沉淀生成,①当AlCl3过量时,加入NaOH使Al3+部分产生沉淀为0.39 g,通过Al3++3OH-===Al(OH)3↓可知用NaOH 7.5 mL。
②当NaOH过量时,Al3+全部参加反应生成Al(OH)3沉淀后又部分溶解,用NaOH 17.5 mL。
答案:(1)滴入15 mL NaOH溶液时AlCl3完全转化为Al(OH)3,沉淀的质量为0.78 g
(2)滴入20 mL NaOH溶液时,生成的Al(OH)3沉淀完全溶解
(3)Al3++4OH-===AlO +2H2O
+2H2O
(4)17.5 mL或7.5 mL


科目:高中化学 来源: 题型:
[化学——有机化学基础](13分)
叶酸是维生素B族之一,可以由下列甲、乙、丙三种物质合成。
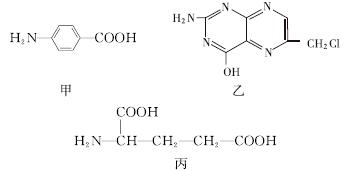
(1)甲中显酸性的官能团是________(填名称)。
(2)下列关于乙的说法正确的是________(填序号)。
a.分子中碳原子与氮原子的个数比是7∶5
b.属于芳香族化合物
c.既能与盐酸又能与氢氧化钠溶液反应
d.属于苯酚的同系物
(3)丁是丙的同分异构体,且满足下列两个条件,丁的结构简式为________。
a.含有H2NCHCOOH
b.在稀硫酸中水解有乙酸生成
(4)甲可以通过下列路线合成(分离方法和其他产物已经略去):
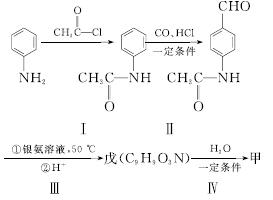
①步骤Ⅰ的反应类型是________。
②步骤Ⅰ和Ⅳ在合成甲过程中的目的是________。
③步骤Ⅳ反应的化学方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
过氧化氢是一种常见绿色氧化剂,用途广泛,其水溶液俗称双氧水。
(1)已知液态过氧化氢与水相似,可微弱电离,得到两种等电子微粒。请写出过氧化氢的电离方程式__________________。
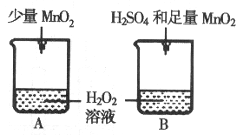
(2)如图所示:两个盛有等量过氧化氢溶液的容器A和B,向A中加入少量MnO2;向B中加入H2SO4和足量MnO2。充分反应后,B中放出气体的量是A中放出气体的2倍(相同状况),则B中反应的化学方程式是_________;原因是_________。
(3)火箭推进器中盛有强还原剂肼(N2H4)和强氧化剂液态双氧水(H2O2)。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热。已知:0.4 mol液态肼与足量的液态双氧水反应放出256.0 kJ的热量。则该反应的热化学方程式是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
只用一种试剂,将NH4Cl、(NH4)2SO4NaCl、Na2SO4四种溶液区分开,这种试剂是( )
A、NaOH溶液
B、AgNO3溶液
C、BaCl2溶液
D、Ba(OH)2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
将某份铁铝合金样品均分为两份,一份加入足量盐酸,另一份加入足量NaOH溶液,同温同压下产生的气体体积比为3∶2,则样品中铁、铝物质的量之比为( )
A.3∶2 B.2∶1
C.3∶4 D.4∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
将5.4 g Al投入200.0 mL 2.0 mol/L的某溶液中有氢气产生,充分反应后有金属剩余。该溶液可能为( )
A.HNO3溶液 B.Ba(OH)2溶液
C.H2SO4溶液 D.HCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:

请回答下列问题:
(1)流程 甲加入盐酸后生成Al3+的离子方程式为___________________________
甲加入盐酸后生成Al3+的离子方程式为___________________________
________________________________________________________________________。
(2)流程乙加入烧碱后生成SiO 的离子方程式为
的离子方程式为
________________________________________________________________________。
(3)验证滤液B含Fe3+,可取少量滤液并加入__________________(填试剂名称)。
(4)滤液E、K中溶质的主要成分是________(填化学式),写出该溶质的一种用途________________________________________________________________________。
(5)已知298 K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12。取适量的滤液B,加入一定量的烧碱至达到沉淀溶解平衡,测得pH=13.00,则此温度下残留在溶液中的c(Mg2+)=__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-Q kJ·mol-1 (Q>0),下列说法正确的是( )
2SO3(g) ΔH=-Q kJ·mol-1 (Q>0),下列说法正确的是( )
A.相同条件下,2 mol SO2(g)和1 mol O2(g)所具有的能量小于2 mol SO3(g)所具有的能量
B.将2 mol SO2(g)和1 mol O2(g)置于一密闭容器中充分反应后,放出热量为Q kJ
C.增大压强或升高温度,该平衡都向逆反应方向移动
D.将一定量SO2(g)和O2(g)置于密闭容器中充分反应放热Q kJ,此时有2 mol SO2(g)被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关中和滴定的操作:①用标准液润洗滴定管;②往滴定管内注入标准溶液;③检查滴定管是否漏水;④滴定;⑤滴加指示剂于待测液;⑥洗涤。正确的操作顺序是 ( )
A. ⑥③①②⑤④ B. ⑤①②⑥④③
C. ⑤④③②①⑥ D. ③①②④⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com