
| A | B |
| C | D |
| A. | 原子半径:C>A=D>B | |
| B. | 最高价氧化物对应的水化物酸性:B>D | |
| C. | 气态氢化物的稳定性:C>D>B | |
| D. | C的气态氢化物的水溶液在空气中放置会出现浑浊现象,可以说明非金属性A>C |
分析 设A的原子序数为a,则B是a+1,D是a+9,因为A、B原子序数之和与D的原子序数相等,即2a+1=a+9,则a=8,所以A是氧、B是氟、C是硫、D是氯;
A、电子层数越多半径越大,电子层相同时核电荷数越多半径越小;
B、非金属性越强最高价氧化物对应的水化物的酸性越强;
C、中心元素非金属性越强气态氢化物越稳定;
D、氢化物是硫化氢的水溶液放置在空气中会变浑浊,说明氧气能氧化硫化氢,则氧气的氧化性大于S;
解答 解:设A的原子序数为a,则B是a+1,D是a+9,因为A、B原子序数之和与D的原子序数相等,即2a+1=a+9,则a=8,所以A是氧、B是氟、C是硫、D是氯;
A、电子层数越多半径越大,电子层相同时核电荷数越多半径越小,所以半径C>D>A>B,故A错误;
B、氟无最高价,故B错误;
C、非金属氟>氯>硫,所以氢化物的稳定性B>D>C,故C错误;
D、氢化物是硫化氢的水溶液放置在空气中会变浑浊,说明氧气能氧化硫化氢,则氧气的氧化性大于S,所以非金属性A>C,故D正确;
故选D.
点评 本题考查了元素周期律、元素周期表的综合应用,正确推断元素是解本题关键,结合元素周期律来分析解答,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 40K和40Ca原子中的质子数和中子数都相等 | |
| B. | 某元素原子最外层只有两个电子,它一定是金属元素 | |
| C. | 任何原子或离子的组成中都含有质子 | |
| D. | 同位素的不同核素物理、化学性质完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用电子式表示氯化氢分子的形成过程: | |
| B. | 一定条件下从正反应开始的某可逆反应达到化学平衡时,正反应速率降到最小 | |
| C. | 酸与碱发生中和反应时放出的热量叫中和热 | |
| D. | 催化剂不但能改变反应速率,也能改变反应进行的限度 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
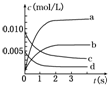 在2L密闭容器内,800℃时反应2SO2(g)+O2(g)=2SO3(g)体系中,n(SO2)随时间的变化如下表:
在2L密闭容器内,800℃时反应2SO2(g)+O2(g)=2SO3(g)体系中,n(SO2)随时间的变化如下表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(SO2)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
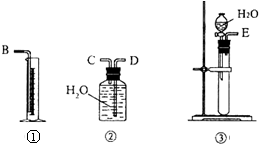 现有含CaO杂质的CaC2试样.某研究性学习小组的同学用图中的装置,设计一个实验,测定CaC2试样的纯度.
现有含CaO杂质的CaC2试样.某研究性学习小组的同学用图中的装置,设计一个实验,测定CaC2试样的纯度.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 还原性:X的氢化物>Y的氢化物>Z的氢化物 | |
| B. | 简单离子的半径:M的离子>Z的离子>Y的离子>X的离子 | |
| C. | YX2与M2Y的水溶液在酸性条件下不能反应 | |
| D. | Z元素最高价氧化物对应的水化物的化学式为HZO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
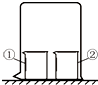 用图所示装置进行下列实验,实验结果与预测现象不一致的是( )
用图所示装置进行下列实验,实验结果与预测现象不一致的是( )| 选项 | ①中物质 | ②中物质 | 预测现象 |
| A | 酚酞溶液 | 浓氨水 | ①中无色变红色 |
| B | CCl4 | 液溴 | ①中变橙色 |
| C | 浓氨水 | 浓硫酸 | 空气中产生白烟 |
| D | NaAlO2溶液 | 浓盐酸 | ①中有白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com