
A、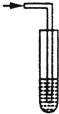 |
B、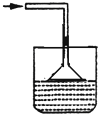 |
C、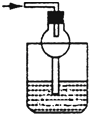 |
D、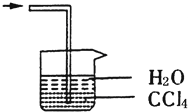 |


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
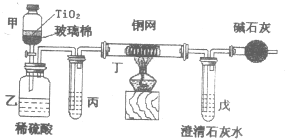
 利用常温下氨气与氯气能发生置换反应的性质,在氯碱工业生产中用氨来检查氯气是否泄漏,其模拟装置如图.下列有关说法不正确的是( )
利用常温下氨气与氯气能发生置换反应的性质,在氯碱工业生产中用氨来检查氯气是否泄漏,其模拟装置如图.下列有关说法不正确的是( )| A、烧瓶中会出现白烟 |
| B、烧瓶中会立即出现喷泉 |
| C、烧瓶中发生的反应表明常温下氨气有还原性 |
| D、烧瓶内氨气与氯气发生的反应中,氧化剂与还原剂物质的量之比是3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCN的结构式:H-C≡N |
B、HClO的电子式为: |
C、HOCH2COOH缩聚物的结构简式: |
D、2-氯甲苯的结构简式: |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯化镁、氢氧化钠 |
| B、硫酸钠、氢氧化钡 |
| C、碳酸氢钠、氢氧化钡 |
| D、氯化铝、氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、K+、S2-、Cl- |
| B、Al3+、Mg2+、SO42-、Cl- |
| C、K+、Fe2+、AlO2-、NO3? |
| D、K+、Na+、SO42-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(HCN)<c(CN-) |
| B、c(Na+)=c(CN-) |
| C、c(HCN)-c(CN-)=c(OH-) |
| D、c(HCN)+c(CN-)=0.1 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、D、E、W是元素周期表前四周期中常见的元素,其相关信息如下表:
A、B、D、E、W是元素周期表前四周期中常见的元素,其相关信息如下表:| 元素 | 相关信息 |
| A | A原子L层电子数是K层电子数的2倍 |
| B | B是地壳中含量最多的元素 |
| D | 在第3周期元素中,它的简单离子半径最小 |
| E | E存在质量数为23,中子数为12的核素 |
| W | W有多种化合价,其白色氢氧化合物在空气中会迅速变成灰绿色,最后变成红褐色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com