
【题目】常见的有机物A、B、C、D、E、F间的转换关系如图所示(以下变化中,某些反应条件及产物未标明)。B是天然有机高分子化合物,C、D可发生银镜反应。

(1)B的分子式为_______________;F的结构简式为_________。
(2)E中官能团的名称是____________。
(3)A的同分异构体的结构简式是_____________。
(4)A→D反应的化学方程式:__________。
(5)D→E反应的化学方程式:_____________。
【答案】(C6H10O5)n CH3COOC2H5 羧基 CH3OCH3 2CH3CH2OH+O2![]() 2CH3CHO+2H2O 2CH3CHO+O2
2CH3CHO+2H2O 2CH3CHO+O2![]() 2CH3COOH
2CH3COOH
【解析】
因为B是天然有机高分子化合物,根据B转化为C的条件可知B发生了水解反应,再结合C、D可发生银镜反应(说明C和D分子中有醛基),可以推断B可能是淀粉或纤维素,C为葡萄糖,可以确定A为乙醇,D为乙醛,E为乙酸,F为乙酸乙酯。据此判断。
(1)B为淀粉或纤维素,分子式为(C6H10O5)n;F是乙酸乙酯,结构简式为CH3COOCH2CH3。
(2)E是乙酸,其中官能团的名称是羧基。
(3)A的同分异构体为二甲醚,二甲醚的结构简式为CH3OCH3。
(4)A→D反应的化学方程式为2CH3CH2OH+O2![]() 2CH3CHO+2H2O。
2CH3CHO+2H2O。
(5)D→E反应的化学方程式为2CH3CHO+O2![]() 2CH3COOH。
2CH3COOH。


 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种短周期元素的原子序数依次增大。已知A、C、F位于同一周期,三种元素原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水,D元素原子的最外层电子数比次外层电子数少4个,E元素原子的次外层电子数比最外层电子数多3个。试回答:
(1)写出下列元素的元素符号:
A_____,C_____,D_____,E__________
(2)用电子式表示B、F形成的化合物_____。
(3)A、C两种元素最高价氧化物的水化物之间反应的化学方程式为_____, C、F两种元素最高价氧化物的水化物之间反应的离子方程式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.物质燃烧总是放热的
B.放热反应在反应发生时都不需要加热
C.热化学方程式中,化学式前的化学计量数仅表示物质的量
D.大多数化合反应是放热的,大多数分解反应是吸热的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】哪些共价键是δ键,哪些共价键是π键呢?一般规律是:共价________是δ键;而共价双键中有________δ键,另一个是________,共价三键由________δ键和________π键组成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在试管a中先加入2mL 95%的乙醇,边摇动边缓缓加入5mL浓H2SO4并充分摇匀,冷却后再加入2g无水醋酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管b中加入7mL饱和碳酸钠溶液。连接好装置,用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验。
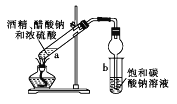
(1)写出a试管中的主要化学反应的方程式________________.
(2)加入浓H2SO4的目的是______________________________.
(3)试管b中观察到的现象是_______________________.
(4)在实验中球形干燥管除了起冷凝作用外,另一个重要作用是______________,其原因_____________.
(5)饱和Na2CO3溶液的作用是______________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.根据下表所示化学反应与数据关系,回答下列问题:
化学反应 | 平衡常数 | 温度 | |
973 K | 1173 K | ||
①Fe(s)+CO2(g)FeO(s)+CO(g) | K1 | 1.50 | 2.15 |
②Fe(s)+H2O(g)FeO(s)+H2(g) | K2 | 2.40 | 1.67 |
③CO(g)+H2O(g)CO2(g)+H2(g) | K3 | ? | ? |
(1)反应①是________(填“吸热”或“放热”)反应。
(2)在973K时,K3=_________。
(3)要使反应③在一定条件下建立的平衡向逆反应方向移动,可采取的措施有______(填写字母序号)。
A.缩小反应容器的容积 B.扩大反应容器的容积 C.升高温度
D.使用合适的催化剂 E.设法减小平衡体系中的CO浓度
Ⅱ.无机和有机氰化物在工农业生产中应用广泛,尤其是冶金工业常用的氰化物,含氰废水的处理显得尤为重要。含氰废水中的氰化物常以[Fe(CN)6]3-和CN-的形式存在,工业上有多种废水处理方法。
(1)电解处理法:
用如图所示装置处理含CN-废水时,控制溶液pH为9~10并加入NaCl,一定条件下电解,阳极产生的ClO-将CN-氧化为无害物质而除去。铁电极为__________(填“阴极” 或“阳极”),阳极产生ClO-的电极反应为__________________________,阳极产生的ClO-将CN-氧化为无害物质而除去的离子方程式为__________________________。
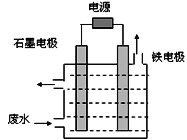
(2)UV(紫外光线的简称)—H2O2氧化法。
实验过程:取一定量含氰废水,调节pH,加入一定物质的量的H2O2,置于UV工艺装置中,
光照一定时间后取样分析。
【查阅资料】
①在强碱性溶液中4[Fe(CN)6]3-+4OH-===4[Fe(CN)6]4-+O2↑+2H2O,[Fe(CN)6]4-更稳定;
②[Fe(CN)6]3-转化为CN-容易被H2O2除去;
③HCN是有毒的弱酸,易挥发。
【问题设计】
①请写出HCN的电子式________________。
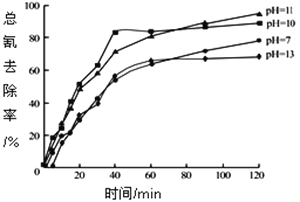
②含氰废水在不同pH下的除氰效果如图所示,pH选择的最佳范围应为________________(选填编号:![]() .7~10;
.7~10;![]() .10~11;
.10~11;![]() .11~13),解释该pH不宜太大的原因___________________。
.11~13),解释该pH不宜太大的原因___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表示细胞四种有机物的组成,依据主要功能,分析回答:
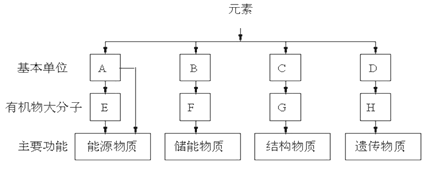
(1)A是指______;E在动物中是指_________,植物中主要是指_________。
(2)F是指_____,它是由B(脂肪酸和甘油)形成的;除此之外,脂质还包括_____和_____。
(3)C是指________;通式是__________,C形成G过程的反应叫_________。
(4)D是指_________,D形成____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,根据要求回答下列问题。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
2 | E | H | F | I | ||||
3 | A | C | D | G | R | |||
4 | B |
(1)十种元素中化学性质最不活泼的元素是________(填元素符号)。
(2)A、C、D三种元素的氧化物对应的水化物,其中碱性最强的是________(填化学式)。
(3)I元素跟A元素形成化合物的是_____(离子或共价)化合物。并用电子式表示该化合物的形成过程_____
(4)G的单质和B的最高价氧化物对应水化物反应的离子方程式是__________________。
(5)元素A和F能形成两种化合物,写出其中较稳定的化合物与CO2反应生成氧气的化学方程式 ______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com