
少量铁片与100mL 0.01mol/L的稀盐酸反应,反应速率太慢。为了加快此反应速率而不改变H2的产量,可以使用如下方法中的
①加H2O ②加KN O3溶液 ③滴入几滴浓盐酸 ④加入少量铁粉 ⑤加NaC
O3溶液 ③滴入几滴浓盐酸 ④加入少量铁粉 ⑤加NaC l溶液 ⑥滴入几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发) ⑧改用10mL 0.1mol/L盐酸
l溶液 ⑥滴入几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发) ⑧改用10mL 0.1mol/L盐酸
A.①⑥⑦ B.③⑤⑧ C.③⑦⑧ D.③④⑥⑦⑧
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源:2017届宁夏高三上学期第三次月考化学试卷(解析版) 题型:选择题
已知A、B、D、E均为化学中的常见物质,它们之间的转化关系如图所示(部分产物略去),则下列有关物质的推断不正确的是( )

A.若A是铁,则E可能为稀硝酸
B.若A是CuO,E是碳,则B为CO
C.若A是NaOH溶液,E是CO2,则B为NaHCO3
D.若A是AlCl3溶液,E可能是氨水
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上12月月考化学试卷(解析版) 题型:实验题
高氯酸铵可用于火箭推进剂,实验室可由NaClO3等原料制取(部分物质溶解度如图),其实验流程如下:
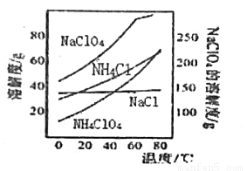
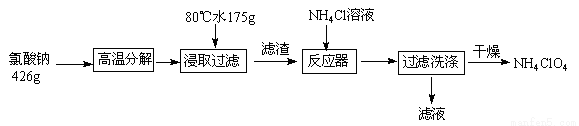
(1)氯酸钠受热分解生成高氯酸钠和氯化钠的化学方程式为_______________。
(2)80℃时浸取液冷却至0℃过滤,滤渣的主要成分为_________________(写化学式)。
(3)反应器中加入氯化铵饱和溶液发生反应的离子方程式为 _____________________。
(4)已知:2NH4ClO4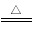 N2↑+2O2↑+Cl2↑+4H2O,现可提供下列试剂:
N2↑+2O2↑+Cl2↑+4H2O,现可提供下列试剂:
a.饱和食盐水 b.浓H2SO4 c.NaOH溶液 d.Mg e.Cu f.Fe
利用下图装置对高氯酸铵热分解产生的三种气体进行分别吸收或收集。

①E中收集到的气体可能是__________________(填化学式)
②A、B、C中盛放的药品依次可以是__________(选填:“I”“II”“III”)。
I.abd II.cbe III.bcf
(5)过滤用到的主要玻璃仪器是____________________。
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上12月月考化学试卷(解析版) 题型:选择题
从下列实验事实所列出的相应结论不正确的是
实 验事实 | 结 论 | |
① | SO2使酸性高猛酸钾溶液褪色 | 可证明SO2有漂白性 |
② | 浓盐酸可除去烧瓶内残留的MnO2,稀硝酸可除去试管内壁的银镜,用硫磺粉处理洒落的金属汞 | 都发生了氧化还原反应 |
③ | 取少Na2SO3样品加入Ba(NO3)2溶液后,产生白色沉淀,再滴加稀盐酸,沉淀不溶解 | 证明Na2SO3己氧化变质 |
④ | 某溶液加入稀盐酸产生能使澄清石灰水变浑浊的气体,另取该溶液滴加CaCl2溶液,有白色沉淀生成 | 确定该溶液存在CO32- |
⑤ | 在某溶液中加入适量新制饱和氯水,再加入CCl4震荡,CCl4层呈橙红色 | 该溶液一定有Br-存在 |
A.①③④ B.②③⑤ C.④⑤ D.③④
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上12月月考化学试卷(解析版) 题型:选择题
工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g) Si(s)+4HCl(g) ΔH=Q kJ/mol(Q>0),某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是
Si(s)+4HCl(g) ΔH=Q kJ/mol(Q>0),某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1 mol, 则达平衡时,吸收热量为Q kJ
C.反应至4 min时,若HCl浓度为0. 12 mol/L,则H2的反应速率为0.03 mol/(L·min)
D.当反应吸收热量0.025Q kJ时,生成的HCl通入含0. 1 mol NaOH的溶液恰好反应
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上12月月考化学试卷(解析版) 题型:选择题
某溶液可能含有K+、NH4+、Fe2+、Fe3+、SO42-、CO32-、SiO32-、Cl-、I-中的几种离子,己知各离子的浓度均为0.2mol/L,进行如下实验(不考虑盐类的水解及水的电离):
①取少量该溶液,加入足量稀硫酸,无明显现象。
②取①反应后的溶液,加入足量浓NaOH溶液,最终得到红褐色沉淀,并伴有刺激性气味气体产生。
下列说法不正确的是
A.根据实验①可知溶液中不存CO32-、SiO32-
B.该溶液中肯定存在NH4+、Fe2+
C.该溶液中至少含有4种离子
D.另取该溶液,加入适量氯水和淀粉溶液,若溶液显蓝色,即可确定该溶液中只含NH4+、Fe2+、Fe3+、SO42-、I-
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上12月月考化学试卷(解析版) 题型:选择题
硼化钒(VB2)—空气电池是目前储电能力最高的电池,电池示意图如下,该电池工作时反应为:4VB2 + 11O2 = 4B2O 3 + 2V2O5,下列说法正确的是
3 + 2V2O5,下列说法正确的是
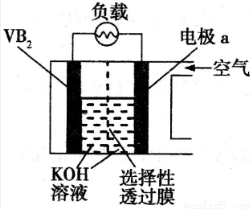
A.电极a为电池负极,发生还原反应
B.每消耗1molVB2转移6mol电子
C.电池工作时,OH‑向电极a移动
D.VB2极发生的电极反应为:2VB2+22OH?-22e?=V2O5+2B2O3+11H2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二12月月考化学试卷(解析版) 题型:选择题
把0.6molX气体和0.4molY气体混合于2L容器中使它们发生如下反应反应: 3X(g)+Y(g)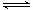 nZ(g)+2W(g);5 min末已生成0.2 mol W,若测知以Z浓度变化来表示的反应速率为0.01 mol/( L·min),则上述反应中Z气体的反应方程式中化学计量系数n的值是
nZ(g)+2W(g);5 min末已生成0.2 mol W,若测知以Z浓度变化来表示的反应速率为0.01 mol/( L·min),则上述反应中Z气体的反应方程式中化学计量系数n的值是
A.1 B.2 C.3 D.4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高一期中化学卷(解析版) 题型:选择题
实验中的下列操作正确的是
A. 用滴管取试剂瓶中Na2CO3溶液于试管中,发现取量过多,为了不浪费,又把过量试剂倒入试剂瓶中
B. Ba(NO3)2溶于水,可将含有Ba(NO3)2 的废液倒入水槽中,再用水冲入下水道
C. 用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干
D. 用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com