
| A. | a是一种非金属元素 | |
| B. | b与氧元素组成的氧化物一定是碱性氧化物 | |
| C. | b、c、d与氢元素形成的化合物中化学键均为极性共价键 | |
| D. | c2d2中各原子的最外层均达到8电子稳定结构 |
分析 原子序数依次增大的短周期主族元素a、b、c、d,a的最外层电子数为其质子数的一半,原子只能有2个电子层,设A原子最外层电子数为x,则2x=x+2,则A为Be;b的最外层只有1个电子,原子序数大于Be,则b为Na;c的最高化合价与最低化合价的代数和为4,则c为S元素,故d为Cl.
解答 解:原子序数依次增大的短周期主族元素a、b、c、d,a的最外层电子数为其质子数的一半,原子只能有2个电子层,设A原子最外层电子数为x,则2x=x+2,则A为Be;b的最外层只有1个电子,原子序数大于Be,则b为Na;c的最高化合价与最低化合价的代数和为4,则c为S元素,故d为Cl.
A.A为Be,属于金属元素,故A错误;
B.b与氧元素组成的氧化物有氧化钠、过氧化钠,过氧化钠不属于碱性氧化物,故B错误;
C.b、c、d与氢元素形成的化合物中NaH属于离子化合物,含有离子键,故C错误;
D.S2Cl2结构式为Cl-S-S-Cl,各原子的最外层均达到8电子稳定结构,故D正确.
故选:D.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,金属氢化物为中学盲点,注意金属氢化物的性质,难度中等.


 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 原子序数X>Y>Z | |
| B. | 元素的非金属性由强至弱的顺序是X>Y>Z | |
| C. | 原子半径大小顺序是X>Y>Z | |
| D. | 气态氢化物的稳定性H3X>H2Y>HZ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
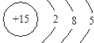 、其最高价氧化物对应的水化物的化学式H3PO4.
、其最高价氧化物对应的水化物的化学式H3PO4.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X、Y、Z的稳定性逐渐减弱 | |
| B. | A、B、C、D只能形成5种单质 | |
| C. | X、Y、Z三种化合物的熔沸点逐渐升高 | |
| D. | 由A、B、C、D四元素间形成的化合物中只含共价键,不含离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
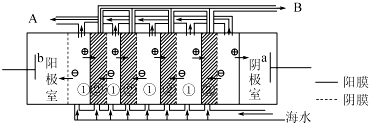
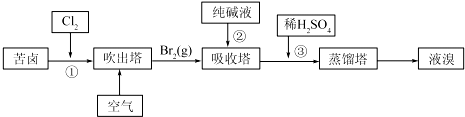
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 五种元素的原子半径从大到小的顺序是:M>W>Z>Y>X | |
| B. | X、Z两元素能形成原子个数比(X:Z)为3:1的化合物 | |
| C. | 化合物YW2、ZW2都是酸性氧化物 | |
| D. | 用M单质作阳极,石墨作阴极,电解NaHCO3溶液,电解一段时间后,在阴极区会出现白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 干冰的主要成分是H2O | B. | 吸入CO可导致人体中毒 | ||
| C. | SO2可大量用于漂白食品 | D. | 小苏打的主要成份是Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 埋在潮湿土壤里的铁管比在干燥土壤中的更易被腐蚀 | |
| B. | 在空气中,金属镁、铝的表面可形成一层氧化膜 | |
| C. | 为保护海轮的船壳,常在海轮上镶嵌锌块 | |
| D. | 镀锡的铁制品,镀层部分破坏后,露出的铁表面更容易被腐蚀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com