
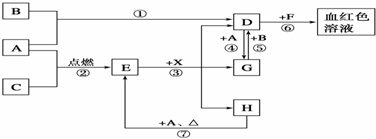
分析 A为固体,B为黄绿色气体,说明B为Cl2,D与F反应得到血红色溶液,结合转化关系可知,固体A为Fe,D为FeCl3,F为KSCN,由D与G之间的相互转化,可知G为FeCl2,Fe与无色气体C反应得到E,E与X反应得到D、G、H,且X常温下是无色气体,其水溶液是一种强酸,E为黑色固体,H在常温下为液体,可推知C为O2,E为Fe3O4,X为HCl,H为H2O,以此解答该题.
解答 解:A为固体,B为黄绿色气体,说明B为Cl2,D与F反应得到血红色溶液,结合转化关系可知,固体A为Fe,D为FeCl3,F为KSCN,由D与G之间的相互转化,可知G为FeCl2,Fe与无色气体C反应得到E,E与X反应得到D、G、H,且X常温下是无色气体,其水溶液是一种强酸,E为黑色固体,H在常温下为液体,可推知C为O2,E为Fe3O4,X为HCl,H为H2O,
(1)由上述分析可知,A为Fe,D为FeCl3,E为Fe3O4,X为HCl,
故答案为:Fe;FeCl3;Fe3O4;HCl;
(2)反应④的离子方程式是:2Fe3++Fe=3Fe2+,
故答案为:2Fe3++Fe=3Fe2+;
(3)反应⑦是铁在水蒸气中发生的反应生成四氧化三铁和氢气,反应的化学方程式为:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;该反应中符合氧化还原反应的电子守恒,氢元素化合价从+1价变化为0价,4H2O反应转移电子为 8mol,铁元素从0价变化为+$\frac{8}{3}$价,每消耗 0.3mol的A(Fe),可转移电子0.8mol,
故答案为:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;0.8;
(4)D为FeCl3,可与碳酸氢钠发生互促水解反应,反应的离子方程式为Fe3++3HCO3-=Fe(OH)3↓+3CO2↑,故答案为:Fe3++3HCO3-=Fe(OH)3↓+3CO2↑;
(5)除去FeCl3溶液中混有的少量FeCl2的方法是:向混合溶液中通入足量的氯气,故答案为:向混合溶液中通入足量的氯气;
(6)如果要从氯化铁溶液得到纯氯化铁固体,需要抑制氯化铁的水解得到氯化铁,将三氯化铁溶液在HCl环境(或气氛)中加热蒸干,
故答案为:将三氯化铁溶液在HCl环境(或气氛)中加热蒸干.
点评 本题考查无机物推断,为高频考点,侧重于学生的分析能力的考查,涉及Fe、Cl元素化合物的性质与转化,物质的颜色是推断突破口,需要熟练掌握元素化合物知识,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
| ① | ② | ③ | ||
| ④ | ⑤ | ⑥ | ⑦ |
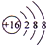 、
、 ,这两种离子的半径大小顺序是S2->Cl-(填化学式).
,这两种离子的半径大小顺序是S2->Cl-(填化学式).查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 所需仪器有:100mL容量瓶、烧杯、玻璃棒、胶头滴管、托盘天平 | |
| B. | 将量取的浓盐酸先倒入容量瓶,再加入蒸馏水至刻度线,摇匀 | |
| C. | 将溶液转移入容量瓶,要用玻璃棒引流 | |
| D. | 定容时仰视刻度,所配溶液浓度偏小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某气体$\stackrel{通入品红溶液中}{→}$品红溶液褪色 结论:某气体一定是SO2 | |
| B. | 某气体$\stackrel{通入澄清石灰水}{→}$ 产生白色沉淀 结论:某气体一定是CO2 | |
| C. | 某溶液$\stackrel{打开瓶盖}{→}$冒白雾$\stackrel{将沾有浓氨水的玻璃棒靠近}{→}$ 白烟 结论:原溶液一定是浓盐酸 | |
| D. | 某溶液$\stackrel{滴加KSCN溶液液}{→}$ 血红色溶液 结论:原溶液中一定含有Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X中一定不存在FeO | |
| B. | Y中一定含有MnO2,Fe2O3 | |
| C. | Z溶液中一定含有Na2SO4,不能确定是否含有AlCl3 | |
| D. | 不溶物Y中一定含有Fe和CuO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn | B. | Fe | C. | Mg | D. | Al |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
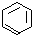 、④HCHO,其中碳原子采取sp2杂化的分子有①③④(填物质编号),HCHO分子的立体构型为平面三角形.
、④HCHO,其中碳原子采取sp2杂化的分子有①③④(填物质编号),HCHO分子的立体构型为平面三角形.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com