


科目:高中化学 来源: 题型:
| A、与28 g CO具有相同分子数的CO2的质量一定是44 g |
| B、在标准状况下,11.2 L某气体的质量为22 g,则该气体的相对分子质量是44 g/mol |
| C、16 g O2和16 g O3含的氧原子个数一样多 |
| D、1 L 1 mol?L-1Fe(OH)3胶体中胶体微粒数目小于NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、生成物的总能量总是低于反应物的总能量 |
| B、应用盖斯定律,可计算某些难以直接测量的反应热 |
| C、化学反应中的能量变化都表现为热量变化 |
| D、需要加热才能发生的反应一定是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验步骤 | 实验现象 |
| ①取少量原溶液,加入稀盐酸, | 产生无色气体,该气体能使澄清的石灰水变浑浊 |
| ②取少量原溶液加热浓缩,加入Cu片和一定浓度的H2SO4 | 有无色气体产生,该气体遇空气变成红棕色 |
| ③取少量原溶液,加入BaCl2溶液 | 有白色沉淀生成 |
| ④取③中上层清液,先加入稀硝酸,再加入AgNO3溶液 | 有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
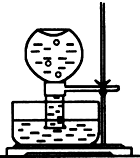 (1)如图所示,现有一瓶饱和氯水倒扣于水槽中,当日光照射到盛有氯水的装置时,可观察到平底烧瓶内有气泡产生,放置一段时间后溶液颜色变浅,产生上述现象的原因是(请用相关的反应方程式和简要文字说明)
(1)如图所示,现有一瓶饱和氯水倒扣于水槽中,当日光照射到盛有氯水的装置时,可观察到平底烧瓶内有气泡产生,放置一段时间后溶液颜色变浅,产生上述现象的原因是(请用相关的反应方程式和简要文字说明)查看答案和解析>>
科目:高中化学 来源: 题型:
| 操作 | 现象 |
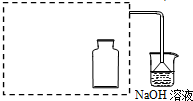
| a.用干燥洁净的烧杯取约10mL浓硝酸,加热. |  |
| b.把小块烧红的木炭迅速伸入热的浓硝酸中. | 红热的木炭与热的浓硝酸接触发生剧烈反应,同时有大量红棕色气体产生,液面上木炭迅速燃烧,发出光亮. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com