
|
将钠在干燥的空气中形成的氧化物1.4 g溶于水后,可被80 mL 0.5 mol/L盐酸恰好中和,钠的氧化物的成分是 | |
| [ ] | |
A. |
Na2O |
B. |
Na2O与Na2O2 |
C. |
Na2O2 |
D. |
Na2O与Na2O |
科目:高中化学 来源:广东省珠海二中2008-2009学年高二下学期6月月考化学试题 题型:058
环己酮(微溶于水,易溶于醇和醚,沸点155.7℃)是一种重要的有机化工原料,主要用于制造己内酰胺和己二酸.实验室可用环己醇氧化制取环己酮(已知该反应为放热反应):

实验步骤如下:
①将重铬酸钠溶于适量水,边搅拌边慢慢加入浓H2SO4,将所得溶液冷至室温备用.
②在一圆底烧瓶(乙)中加入适量环己醇,并将①中溶液分三次加入圆底烧瓶,每加一次都应振摇混匀.控制瓶内温度在55℃~60℃之间,充分反应0.5 h.
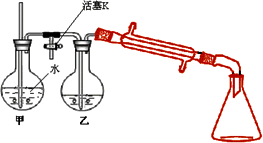
③向②反应后的圆底烧瓶内加入少量水,并接入右图所示装置中,将T形管的活塞K打开,甲瓶中有适量水,加热甲,至有大量水蒸气冲出时关闭K,同时接通冷凝水.
④将步骤③锥形瓶中收集到的液体分液,水层用乙醚(乙醚沸点34.6℃,易燃烧,当空气中含量为1.83~48.0%时易发生爆炸)萃取,萃取液并入有机层.再向有机层中加入无水硫酸钠静置后转入干燥的圆底烧瓶中,进行蒸馏,除去乙醚后收集151℃~155℃馏分.
根据以上步骤回答下列问题:
(1)步骤①所得溶液分三次加入环己醇的原因是________.
(2)步骤③利用图示装置进行实验的目的是________,实验过程中要经常检查甲中玻璃管内的水位.若玻璃管内的水位升高过多,其可能原因是________,此时应立即采取的措施是________.
(3)步骤④中加入无水硫酸钠的作用是________,蒸馏除乙醚的过程中采用的加热方式为________.
(4)写出该实验中可能发生的一个副反应的化学方程式________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com