
 药物阿司匹林可由水杨酸制得,它们的结构如图所示,有关说法正确的( )
药物阿司匹林可由水杨酸制得,它们的结构如图所示,有关说法正确的( )| A. | 服用阿司匹林,身体出现水杨酸不良反应时,可静脉注射NaHCO3溶液 | |
| B. | 阿司匹林的分子式为C9H10O4 | |
| C. | 1mol阿司匹林最多可消耗2molNaOH | |
| D. | 水杨酸可以发生取代,加成,氧化,加聚反应 |
分析 A.水杨酸含-COOH,可与碳酸氢钠反应;
B.由结构可知分子式;
C.-COOH、-COOC-及水解生成的酚-OH均与NaOH反应;
D.水杨酸含酚-OH、-COOH.
解答 解:A.水杨酸含-COOH,可与碳酸氢钠反应,则身体出现水杨酸不良反应时,可静脉注射NaHCO3溶液,故A正确;
B.由结构可知阿司匹林的分子式为C9H8O4,故B错误;
C.-COOH、-COOC-及水解生成的酚-OH均与NaOH反应,则1mol阿司匹林最多可消耗3molNaOH,故C错误;
D.水杨酸含酚-OH含发生取代、氧化反应,含苯环可发生加成反应,但不能发生加聚反应,故D错误;
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物官能团与性质的关系为解答的关键,侧重酚、酯性质的考查,选项C为解答的难点,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Kb(NH3•H2O) | B. | n(OH-) | C. | $\frac{{c({N{H_3}•{H_2}O})}}{{c({O{H^-}})}}$ | D. | $\frac{{c({O{H^-}})}}{{c({NH_4^+})}}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg3N2与盐酸反应能生成两种盐 | B. | CaC2的水解产物是Ca(OH)2和C2H2 | ||
| C. | Si3N4的水解产物之一是H2SiO3 | D. | PCl5的水解产物是HClO和PH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
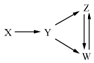 一定条件下,下列各组物质能一步实现如图所示转化关系的是( )
一定条件下,下列各组物质能一步实现如图所示转化关系的是( )| 选项 | X | Y | Z | W |
| A | Al | Al2O3 | NaAlO2 | Al(OH)3 |
| B | Fe2O3 | Fe | FeCl2 | FeCl3 |
| C | H2SO4 | SO2 | S | SO3 |
| D | NH3 | N2 | NO | NO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单位对间内消耗2mol的CO同时生成2mol的CO2 | |
| B. | 两个H-O键断裂的同时有一个H-H键断裂 | |
| C. | 反应容器内的压强不再发生变化 | |
| D. | 混合气体的相对分子质量不发生变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com