
| A、40K与40Ca |
| B、T2O和H2O |
| C、40K与39K |
| D、金刚石与石墨 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、麦芽糖及其水解产物均能与新制的Cu(OH)2悬浊液反应 |
| B、棉、丝、毛、油脂都是天然有机高分子化合物 |
| C、白菜上洒少许福尔马林,既保鲜又消毒 |
| D、石英玻璃、陶瓷都属于硅酸盐产品 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,pH=7的硫酸铵和氨水混合溶液中:2c(NH4+)=c(SO42-) |
| B、常温下,0.1mol?L-1的硫酸氢钠、碳酸氢钠、碳酸钠溶液中,水电离出的c(OH-)依次增大 |
| C、在空气中蒸干硫酸铝溶液、硫酸亚铁溶液、氯化镁溶液可以得到对应的无水盐 |
| D、同温、同浓度的①氯化铵、②硫酸氢铵、③碳酸氢铵溶液中c(NH4+):①>③>② |
查看答案和解析>>
科目:高中化学 来源: 题型:
283 116 |
| A、这种原子的中子数为167 |
| B、它位于元素周期表中第六周期 |
| C、这种元素一定是金属元素 |
| D、这种元素的原子易与氢化合 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
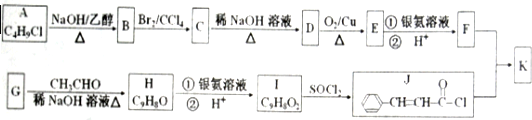

查看答案和解析>>
科目:高中化学 来源: 题型:
 室温下,把SiO2超细粉置入蒸馏水中,不断搅拌至平衡,形成 H4SiO4溶液,反应原理如下:SiO2(s)+2H2O(l)?H4SiO4(aq)△H.
室温下,把SiO2超细粉置入蒸馏水中,不断搅拌至平衡,形成 H4SiO4溶液,反应原理如下:SiO2(s)+2H2O(l)?H4SiO4(aq)△H.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com