
【题目】硫化钠是重要的化工原料,大多采用无水芒硝(Na2SO4)—炭粉还原法制备,原理为:Na2SO4+2CNa2S+2CO2↑。其主要流程如下:

(1) 上述流程中采用稀碱液比用热水更好,理由是________________________________________________________________________。
(2) 已知:I2+2S2O32-===2I-+S4O62-。所制得的Na2S·9H2O晶体中含有Na2S2O3·5H2O等杂质。为测定产品的成分,进行下列实验,步骤如下:
a. 取试样10.00 g配成500.00 mL溶液。
b. 取所配溶液25.00 mL于碘量瓶中,加入过量ZnCO3悬浊液除去Na2S后,过滤,向滤液中滴入2~3滴淀粉溶液,用0.050 00 mol·L-1 I2溶液滴定至终点,用去5.00 mL I2溶液。
c. 再取所配溶液25.00 mL于碘量瓶中,加入50.00 mL 0.050 00 mol·L-1的I2溶液,并滴入2~3滴淀粉溶液,振荡。用标准Na2S2O3溶液滴定多余的I2,用去15.00 mL 0.100 0 mol·L-1 Na2S2O3溶液。
①步骤b中用ZnCO3除去Na2S的离子方程式为____________。
②判断步骤c中滴定终点的方法为______________。
③计算试样中Na2S·9H2O和Na2S2O3·5H2O的质量分数,写出计算过程__________。
【答案】 热水会促进Na2S水解,而稀碱液能抑制Na2S水解 ZnCO3+S2-===ZnS+CO 溶液由蓝色变为无色,且半分钟内不变色。 步骤b中消耗的I2有:
n(I2)=0.050 00 mol·L-1×5.00 mL×10-3 L·mL-1=2.500×10-4 mol
n(Na2S2O3·5H2O)=2n(I2)=5.000×10-4 mol(1分)
w(Na2S2O3·5H2O)=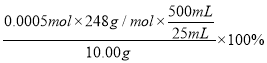
=24.8%(1分)
步骤c中,加入的I2有:
n(I2)=0.050 00 mol·L-1×50.00 mL×10-3 L·mL-1=2.500×10-3 mol(1分)
溶液中Na2S2O3消耗的I2有:2.500×10-4 mol(1分)
滴入的标准Na2S2O3溶液消耗多余的I2有:
15.00 mL×10-3 L·mL-1×0.100 0 mol·L-1×1/2=7.500×10-4 mol
溶液中Na2S有:
n(Na2S)=(2.500×10-3-2.500×10-4-7.500×10-4)mol=1.500×10-3 mol(1分)
w(Na2S·9H2O)=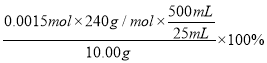
=72.0%(1分)
【解析】(1)硫化钠水解,溶液显碱性,水解吸热,热水会促进Na2S水解,而稀碱液能抑制Na2S水解。(2)①步骤b中用ZnCO3除去Na2S,反应中生成更难溶的ZnS,反应的离子方程式为 ZnCO3+S2-=ZnS+CO32-。②碘遇淀粉显蓝色,则判断步骤c中滴定终点的方法为溶液由蓝色变为无色,且半分钟内不变色。③步骤b中消耗的I2为:
n(I2)=0.050 00 mol·L-1×5.00 mL×10-3 L·mL-1=2.500×10-4 mol
n(Na2S2O3·5H2O)=2n(I2)=5.000×10-4 mol
w(Na2S2O3·5H2O)=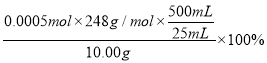 =24.8%
=24.8%
步骤c中,加入的I2有:
n(I2)=0.050 00 mol·L-1×50.00 mL×10-3 L·mL-1=2.500×10-3 mol
溶液中Na2S2O3消耗的I2有:2.500×10-4 mol
滴入的标准Na2S2O3溶液消耗多余的I2有:
15.00 mL×10-3 L·mL-1×0.100 0 mol·L-1×1/2=7.500×10-4 mol
溶液中Na2S有:
n(Na2S)=(2.500×10-3-2.500×10-4-7.500×10-4)mol=1.500×10-3 mol
w(Na2S·9H2O)=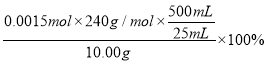 =72.0%
=72.0%


 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案科目:高中化学 来源: 题型:
【题目】短周期元素W、X 、Y 和Z 在周期表中的相对位置如表所示,这四种元素原子的最外层电子数之和为21 。回答下列问题:
W | X | |||
Y | Z |
(1)X 在元素周期表中的位置为_______。
(2)四种元素简单离子的半径由大到小为_____________(用离子符号表达)。
(3)W的最简单氢化物的电子式为________________。
(4)W、Z 最高价氧化物的水化物酸性较强的为___________(填化学式)。
(5)Y单质与Fe2O3 反应能放出大量的热,常用于焊接钢轨,该反应化学方程式为____________________。
(6)向盛有3 mL 鸡蛋清溶液的试管里滴入几滴W的最高价氧化物的水化物浓溶液,实验现象为________________________________________。
(7)C3H7Z 的结构简式有____________________。
(8)ZX2气体是一种广谱杀菌消毒剂。工业上可利用NaZX3和NaZ 在酸性条件下制得ZX2 同时得到Z元素的单质,该反应的离子方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物中碳原子和氢原子个数比为3∶4,不能与溴水反应却能使KMnO4酸性溶液褪色。其蒸气密度是相同状况下甲烷密度的7.5倍。在铁存在时与溴反应,能生成两种一溴代物。该有机物可能是( )

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,已知可逆反应X(g)+3Y(g) ![]() 2Z(g),甲、乙两个恒温恒容的密闭容器中各物质浓度如下表所示:
2Z(g),甲、乙两个恒温恒容的密闭容器中各物质浓度如下表所示:
X(g) | Y(g) | Z(g) | ||
容器甲 | 初始浓度(mol/L) | 2.5 | y | 0 |
平衡浓度(mol/L) | x | 2.0 | 1.0 | |
容器乙 | t时刻浓度(mol/L) | 3.0 | 2.0 | 2.0 |
下列有关正确的是
A. x=3.5,Y=3.5 B. 平衡常数为1/6
C. 乙容器t时刻v(正)(逆) D. 因温度相等,平衡常数相同,故容器甲与容器乙中反应能达到等效平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A.钠和冷水反应:Na+2H2O == Na++2OH-+H2↑
B.金属铝溶于氢氧化钠溶液:Al+2OH-== AlO![]() +H2↑
+H2↑
C.金属铝溶于盐酸中:2Al+6H+ == 2Al3++3H2↑
D.铁跟稀硫酸反应:Fe+2H+ == Fe3++H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是( )
A. 冰融化时,分子中H—O键发生断裂
B. 原子晶体中,共价键越强,熔点越高
C. 分子晶体中,共价键键能越大,该分子晶体的熔沸点一定越高
D. 在晶体中只要有阳离子就一定有阴离子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com