
【题目】过氧化尿素(CO(NH2)2·H2O2)是过氧化氢水溶液与尿素的加和物,兼有尿素和过氧化氢的性质,是一种新型漂白、消毒剂,广泛应用于农业、医药、日用化工等领域。某化学小组同学用低浓度的双氧水和饱和尿素[CO(NH2)2]溶液在30℃条件下用右图装置合成过氧化尿素。请回答下列问题:
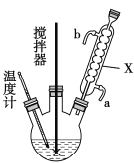
(1)仪器X的名称是______________;
(2)制备过氧化尿素的化学方程式为_______________________,反应时采取的受热方式为_____________;
(3)搅拌器不能选择铁质材料的原因是______________________
(4)过氧化尿素中活性氧含量的高低直接决定产品的质量,合格产品中活性氧的含量≥16%(相当于其中含H2O234%)。为了确定所得产品合格与否,质检员称取干燥样品8.000g,溶解于水,在250mL容量瓶中定容,准确量取其中25.00mL溶液于锥形瓶中,加入1mL6mol·L-1H2SO4,然后用0.2000mol·L-1KMnO4标准溶液滴定样品中的H2O2(KMnO4溶液与尿素不反应)。三次滴定平均消耗KMnO4溶液20.000mL:
①请完善滴定时反应的离子方程式:__MnO![]() +___H2O2+______==_______________
+___H2O2+______==_______________
②若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量_______(填“偏高”、“偏低”或“不变”);
③根据滴定结果确定产品质量_______(填“合格”或“不合格”),活性氧的质量分数为_________。
【答案】球形冷凝管 CO(NH2)2+H2O2=CO(NH2)2·H2O2 水浴加热 H2O2水溶液呈弱酸性,故H2O2可与铁单质反应,进而氧化生成可催化H2O2分解的Fe3+ 2 5 6H+ 2Mn2++8H2O+5O2 偏高 合格 20%
【解析】
本题从物质的制备入手,通过过氧化氢水溶液与尿素反应,可得到)CO(NH2)2·H2O2,在结合仪器的辨别,反应的方程式等知识点进行考查,重点是利用氧化还原反应的原理来测定过氧化尿素中活性氧含量。
(1)根据上图,可知仪器X是球形冷凝管,故答案为:球形冷凝管;
(2)CO(NH2)2·H2O2是过氧化氢水溶液与尿素的加和物,由双氧水和饱和尿素CO(NH2)2反应制备,化学方程式为:CO(NH2)2+H2O2=CO(NH2)2·H2O2,反应温度为30℃,可采取水浴加热的方式,故答案为:CO(NH2)2+H2O2=CO(NH2)2·H2O2;水浴加热;
(3)过氧化氢水溶液呈酸性,会与铁单质反应,生成的金属离子能加快过氧化氢的分解,所以搅拌器不能选择铁质材料,故答案为:H2O2水溶液呈弱酸性,故H2O2可与铁单质反应,进而氧化生成可催化H2O2分解的Fe3+;
(4)①反应中MnO4-是氧化剂,H2O2是还原剂,氧化产物是O2;依据元素化合价变化,锰元素化合价从+7价变化为+2价,过氧化氢中的氧元素化合价从-1价变化为0价,根据电子守恒配平写出离子方程式为:2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2,故答案为:2;5;6H+;2Mn2++8H2O+5O2;
②若滴定前滴定管尖嘴处有气泡,滴定后消失,依据反应的电离关系可知,5×c(标准)×V(标准)=c(待测)×V(待测)×2,测得标准液体积偏大,结果偏高,故答案为:偏高;
③称取干燥样品8.000g,溶解,在250mL容量瓶中定容.准确量取25.00mL于锥形瓶中,加入1mL 6mol/L的硫酸,然后用0.2000mol/L KMnO4标准溶液滴定,至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液20.00mL;依据反应2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2;
2MnO4-~~~~~5H2O2;
2 5
0.0200L×0.2000mol/L 0.01mol
250mL容量瓶中含过氧化氢0.1mol,过氧化氢质量=0.1mol×34g/mol=3.4g,过氧化氢质量分数=3.4g/8g×100%=42.5%,过氧化氢质量分数大于34%;活性氧16%,相当于H2O234%,则活性氧质量分数=16%×42.5%/34%=20%,该产品为合格产品,故答案为:合格;20%;


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在2020年抗击新型冠状病毒肺炎的战役中,涉及很多化学知识。下列说法不正确的是( )
A.含有病毒的飞沫混合在空气中形成气溶胶,气溶胶能产生丁达尔效应
B.二氧化氯泡腾片可作为环境消毒剂,能使病毒失去生理活性
C.口罩的核心材料熔喷布的主要成分是聚丙烯,聚丙烯的链节为
D.疫情期间,“网课"成了我们的主要学习方式,网络光纤的主要成分是晶体硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时有关弱酸的电离平衡常数:则下列有关说法正确的是( )
弱酸化学式 | CH3COOH | HCN | H2CO3 |
电离平衡常数 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
A. 等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa)
B. 冰醋酸中逐滴加水,则溶液的导电性、醋酸的电离程度、pH均先增大后减小
C. NaCN中通入少量CO2发生的化学反应为:NaCN+CO2+H2O=HCN+NaHCO3
D. 稀释HCN溶液过程中,![]() 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究SO2与Fe3+能否发生氧化还原反应,按如图装置进行实验(夹持、加热仪器略),下列说法正确的是
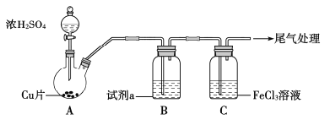
A.铜和浓硫酸反应需要加热的原因是低温下铜被钝化
B.试剂a为饱和NaHSO3溶液,其作用是观察气流速率
C.一段时间,向C中滴加氯化钡溶液,产生白色沉淀,说明Fe3+氧化了SO2
D.一段时间,向C中滴加酸性高锰酸钾,溶液褪色,说明SO2还原了Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】试根据氧化还原反应:2FeCl3+Cu=2FeCl2+CuCl2设计原电池,并画出装置图________________,指出电解质溶液是________________,负极是________________,电极反应式为__________________,正极是___________,电极反应式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式及有关应用的叙述中,正确的是
A. 甲烷的燃烧热为890.3kJmol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+ 2O2(g) ═ CO2(g) + 2H2O(g) △H = -890.3kJmol-1
B. 已知强酸与强碱在稀溶液里反应的中和热为57.3kJmol-1,则![]() H2SO4(aq)+
H2SO4(aq)+![]() Ba(OH)2(aq)═
Ba(OH)2(aq)═![]() BaSO4(s)+H2O(l) △H < -57.3kJmol-1
BaSO4(s)+H2O(l) △H < -57.3kJmol-1
C. 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g) + 3H2(g)![]() 2NH3(g) △H = -38.6kJmol-1
2NH3(g) △H = -38.6kJmol-1
D. 已知25℃、101KPa条件下:4Al(s) + 3O2(g) ═ 2A12O3(s) △H = -2834.9kJmol-1,4Al(s) + 2O3(g) ═ 2A12O3(s) △H = -3119.1kJmol-1,则O3比O2稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1,2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1452 kJ·mol-1,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,下列说法正确的是
A.H2(g)的燃烧热为571.6 kJ·mol-1
B.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多
C.![]() H2SO4(aq)+
H2SO4(aq)+![]() Ba(OH)2(aq)=
Ba(OH)2(aq)=![]() BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
D.3H2(g)+CO2(g)=CH3OH(l)+H2O(l) ΔH=+135.9 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将3mol A与3mol B混合于3L的密闭容器中,发生如下反应:2A(g)+3B(g)![]() 2C(g)+nD(g),2s后达平衡A的转化率为50%,测得v(D)=0.25molL-1s-1,下列推断正确的是( )
2C(g)+nD(g),2s后达平衡A的转化率为50%,测得v(D)=0.25molL-1s-1,下列推断正确的是( )
A.v(B)=0.25molL-1s-1B.C的体积分数为30%
C.B的转化率为25%D.n=2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁铝合金投入100 mL一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为5 mol·L-1的氢氧化钠溶液,生成的沉淀跟加入的氢氧化钠溶液的体积关系如图(横坐标体积单位是mL,纵坐标质量单位是g)。
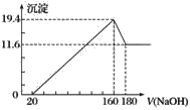
(1)合金中镁的质量是__________。
(2)所用盐酸的物质的量浓度是______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com