
【题目】将铁屑溶于过量的稀盐酸后,再加入下列物质,会有Fe3+生成的是( )
A.硫酸锌B.氯水C.双氧水D.氯化铜
 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源: 题型:
【题目】常温常压下,一氧化二氯(Cl2O)为棕黄色气体,沸点为3.8 ℃,42 ℃以上会分解生成Cl2和O2,Cl2O易溶于水并与水反应生成HClO。
(制备产品)
将氯气和空气(不参与反应)按体积比1∶3混合通入含水8%的碳酸钠中制备Cl2O,并用水吸收Cl2O(不含Cl2)制备次氯酸溶液。

(1)各装置的连接顺序为___→___→___→________→____。___________
(2)装置B中多孔球泡和搅拌棒的作用是_;装置C的作用是__。
(3)制备Cl2O的化学方程式为___。
(4)反应过程中,装置B需放在冷水中,其目的是___。
(5)此方法相对于用氯气直接溶于水制备次氯酸溶液有两个主要优点,分别是____。
(测定浓度)
(6)已知次氯酸可被FeSO4等物质还原。用下列实验方案测定装置E所得溶液中次氯酸的物质的量浓度:量取10 mL上述次氯酸溶液,并稀释至100 mL,再从其中取出10.00 mL于锥形瓶中,并加入10.00 mL 0.80 mol·L-1的FeSO4溶液,充分反应后,用0.050 00 mol·L-1的酸性KMnO4溶液滴定至终点,消耗KMnO4溶液24.00 mL,则原次氯酸溶液的浓度为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.100 0 mol·L-1的盐酸滴定20.00 mL未知浓度的氨水,滴定曲线如图所示,滴加20.00 mL盐酸时所得溶液中c(Cl-)=c(NH4+)+c(NH3·H2O)+c(NH3)。下列说法错误的是

A. 该氨水的浓度为0.100 0 mol·L-1
B. 点①溶液中c(NH4+)+c(NH3·H2O)+c(NH3)=2c(Cl-)
C. 点②溶液中c(NH4+)=c(Cl-)
D. 点③溶液中c(Cl-)>c(H+)>c(NH4+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温恒容时,N2O4 ![]() 2NO2已达平衡状态。现做如下改变:①加入一定量的NO2;②加入一定量的N2O4,二者均再达平衡状态后, NO2和N2O4的物质的量之比值,应( )
2NO2已达平衡状态。现做如下改变:①加入一定量的NO2;②加入一定量的N2O4,二者均再达平衡状态后, NO2和N2O4的物质的量之比值,应( )
A. ①中增大②中减小 B. ①中减小②中增大 C. 均增大 D. 均减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】密闭容器中:xA(g)+yB(g) ![]() zC(g) △H<0,达到平衡后A气浓度为0.5mol/L;恒温下将密闭容器的容积扩大到原来的两倍并再达平衡,测A浓度为0.3 mol/L。下列叙述正确的是( )
zC(g) △H<0,达到平衡后A气浓度为0.5mol/L;恒温下将密闭容器的容积扩大到原来的两倍并再达平衡,测A浓度为0.3 mol/L。下列叙述正确的是( )
A. 平衡向右移动 B. x+y>z C. B的转化率提高 D. C的体积分数增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有两个密闭容器A和B。A容器有一个可以移动的活塞能使容器内保持恒压,B容器能保持恒容。起始时向这两个容器中分别充入1molN2和3mol H2的混合气体,并使A和B容积相等(如下图所示)。在保持400℃的条件下使之发生如下反应:N2(g)+ 3H2(g) ![]() 2NH3(g) 。
2NH3(g) 。
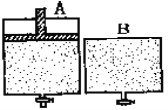
(1)达到平衡时所需的时间:A___ B,N2的转化率:A___B(填“大于”、“小于”或“等于”,下同)
(2)都达平衡后,两容器中分别通入1mol氩气,再达平衡后,N2的转化率:A中_____ B中 _____ (填“增大”、“减小”或“不变”)
(3)都达平衡后,向两容器中再通入1molN2和3mol H2 ,再达到平衡后:混合气体的密度:A中____ B中_____(填“增大”、“减小”或“不变”,下同);混合气体的平均相对分子质量:A中___B中 ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某固定容积的密闭容器中,存在下列化学平衡aA(g) ![]() bB(g)+cC(g),在温度不变的条件下,向容器中再充入一定量的A物质,重新达到平衡时,判断在下列情况下有关物质量的变化趋势(在下列空白中填写“增大”“减小”或“不变”)
bB(g)+cC(g),在温度不变的条件下,向容器中再充入一定量的A物质,重新达到平衡时,判断在下列情况下有关物质量的变化趋势(在下列空白中填写“增大”“减小”或“不变”)
(1)当a=b+c时,B的物质的量分数___________。
(2)当a>b+c时,A的物质的量分数_______。
(3)当a<b+c时,A的转化率___________。
(4)当a<b+c时,混合气体的平均相对分子质量 ___,混合气体的密度 _____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海藻中含有丰富的碘元素(以I形式存在)。实验室中提取碘的流程如下:

(1)实验操作③的名称是________,所用主要仪器名称为________。
(2)提取碘的过程中,可供选择的有机试剂是________(填序号)。
A.酒精(沸点78 ℃) B.四氯化碳(沸点77 ℃)
C.甘油(沸点290 ℃) D.苯(沸点80 ℃)
(3)在操作②中,溶液中生成少量ICl(ICl的性质类似于氯气),为消除此杂质,使碘全部游离出来,应加入适量________(填序号)溶液,反应的离子方程式___________________。
A.KIO3 B.HClO C.KI D.Br2
(4)利用碘的有机溶液得到单质I2的方法是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式书写正确的是(ΔH的绝对值均正确) ( )
A. C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ΔH=-1 367.0 kJ·mol-1(燃烧热)
B. NaOH(aq)+HI(aq)=NaI(aq)+H2O(l) ΔH=-57.3 kJ·mol-1(中和热)
C. S(s)+![]() O2(g)=SO3(g) ΔH=-296.8 kJ·mol-1(燃烧热)
O2(g)=SO3(g) ΔH=-296.8 kJ·mol-1(燃烧热)
D. 2NO2=O2+2NO ΔH=+116.2 kJ·mol-1(反应热)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com