
 äå±½ŹĒŅ»ÖÖ³£ÓĆµÄ»Æ¹¤ŌĮĻ£®ŹµŃéŹŅÖʱøäå±½µÄŹµŃé²½ÖčČēĻĀ£ŗ
äå±½ŹĒŅ»ÖÖ³£ÓĆµÄ»Æ¹¤ŌĮĻ£®ŹµŃéŹŅÖʱøäå±½µÄŹµŃé²½ÖčČēĻĀ£ŗ| ±½ | äå | äå±½ | |
| ĆܶČ/g•cm-3 | 0.88 | 3.10 | 1.50 |
| ·Šµć/”ę | 80 | 59 | 156 |
| ŌŚĖ®ÖŠµÄČܽā¶Č | Ī¢ČÜ | Ī¢ČÜ | Ī¢ČÜ |
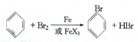 £»
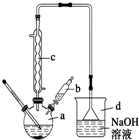
£»·ÖĪö £Ø1£©²½Öč1ŅĒĘ÷aÖŠ£¬±½ÓėŅŗäå·¢ÉśČ”“ś·“Ó¦Öʱøäå±½£»
£Ø2£©ÓÉĶ¼æÉÖŖŅĒĘ÷cµÄĆū³Ę£¬ŅĒĘ÷dĪŖµ¹æŪµÄĀ©¶·£¬ĪüŹÕĘųĢåŹ±æÉ·ĄÖ¹ŅŗĢåµ¹Īü£»
£Ø3£©½«bÖŠµÄŅŗäåĀżĀż¼ÓČėµ½aÖŠ£¬·ĄÖ¹äå»Ó·¢£»
£Ø4£©ŅĒĘ÷cµÄ×÷ÓĆŹĒĄäÄż»ŲĮ÷£¬Ź¹·“Ó¦Īļ¾”æÉÄܳä·Ö·“Ó¦£»
£Ø5£©²½Öč4µĆµ½µÄ“Ö²śĘ·ÖŠ»¹ŗ¬ÓŠŌÓÖŹ±½£¬Óɱ½”¢äå±½µÄÓŠ¹ŲĪļĄķŠŌÖŹæÉÖŖ£¬ŌņŅŖ½ųŅ»²½Ģį“æ“Ö²śĘ·£¬ĄūÓĆ»„ČÜŅŗĢåµÄ·Šµć²»Ķ¬·ÖĄė£»
£Ø6£©ŹµŃé½įŹųŗó£¬Éč¼ĘŹµŃé·½°ø¼ģŃéd×°ÖĆĖłµĆČÜŅŗÖŠŗ¬ÓŠBr-£¬ŠčŅŖĻõĖį”¢ĻõĖįŅų£¬Éś³Éµ»ĘÉ«³Įµķ¼“æÉ£®
½ā“š ½ā£ŗ£Ø1£©²½Öč1ŅĒĘ÷aÖŠ£¬±½ÓėŅŗäå·¢ÉśČ”“ś·“Ó¦Öʱøäå±½£¬·“Ó¦ĪŖ £¬¹Ź“š°øĪŖ£ŗ
£¬¹Ź“š°øĪŖ£ŗ £»
£»
£Ø2£©ÓÉĶ¼æÉÖŖŅĒĘ÷cµÄĆū³ĘĪŖĄäÄż¹Ü£¬ŅĒĘ÷dµÄ×÷ÓĆĪŖĪüŹÕHBr·ĄĪŪČ¾£¬·Ąµ¹Īü£¬
¹Ź“š°øĪŖ£ŗĄäÄż¹Ü£»ĪüŹÕHBr·ĄĪŪČ¾£¬·Ąµ¹Īü£»
£Ø3£©½«bÖŠµÄŅŗäåĀżĀż¼ÓČėµ½aÖŠ£¬¶ų²»ÄÜæģĖŁ¼ÓČėµÄŌŅņŹĒ·ĄÖ¹·“Ó¦·Å³öµÄČČŹ¹C6H6”¢Br2»Ó·¢¶ųÓ°Ļģ²śĀŹ£¬
¹Ź“š°øĪŖ£ŗ·ĄÖ¹·“Ó¦·Å³öµÄČČŹ¹C6H6”¢Br2»Ó·¢¶ųÓ°Ļģ²śĀŹ£»
£Ø4£©ŅĒĘ÷cµÄ×÷ÓĆŹĒĄäÄż»ŲĮ÷£¬Ź¹·“Ó¦Īļ¾”æÉÄܳä·Ö·“Ó¦£¬Ōņ»ŲĮ÷µÄÖ÷ŅŖĪļÖŹÓŠC6H6”¢Br2£¬
¹Ź“š°øĪŖ£ŗC6H6”¢Br2£»
£Ø5£©²½Öč4µĆµ½µÄ“Ö²śĘ·ÖŠ»¹ŗ¬ÓŠŌÓÖŹ±½£¬Óɱ½”¢äå±½µÄÓŠ¹ŲĪļĄķŠŌÖŹæÉÖŖ£¬ŌņŅŖ½ųŅ»²½Ģį“æ“Ö²śĘ·£¬ĄūÓĆ»„ČÜŅŗĢåµÄ·Šµć²»Ķ¬·ÖĄė£¬Ōņ»¹½ųŠŠµÄŹµŃé²Ł×÷Ćū³ĘŹĒÕōĮó£¬
¹Ź“š°øĪŖ£ŗÕōĮó£»
£Ø6£©ŹµŃé½įŹųŗó£¬Éč¼ĘŹµŃé·½°ø¼ģŃéd×°ÖĆĖłµĆČÜŅŗÖŠŗ¬ÓŠBr-£¬ŹµŃé²Ł×÷ĪŖȔɣĮædÖŠČÜŅŗÓŚŹŌ¹ÜÖŠ£¬µĪ¼Ó¹żĮæĻ”HNO3£¬ŌŁ¼ÓČėAgNO3ČÜŅŗ£¬ĻÖĻóŗĶ½įĀŪĪŖÓŠµ»ĘÉ«³ĮµķÉś³É£¬ČÜŅŗÖŠŗ¬ÓŠBr-£¬
¹Ź“š°øĪŖ£ŗȔɣĮædÖŠČÜŅŗÓŚŹŌ¹ÜÖŠ£¬µĪ¼Ó¹żĮæĻ”HNO3£¬ŌŁ¼ÓČėAgNO3ČÜŅŗ£»ÓŠµ»ĘÉ«³ĮµķÉś³É£¬ČÜŅŗÖŠŗ¬ÓŠBr-£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļµÄÖʱøŹµŃ飬ĪŖøßĘµæ¼µć£¬°ŃĪÕÖʱøŹµŃéŌĄķ”¢ŹµŃé¼¼ÄÜ”¢»ģŗĻĪļ·ÖĄėĢį“攢Ąė×Ó¼ģŃéµČĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėŹµŃéÄÜĮ¦µÄ漲飬ĢāÄæÄŃ¶Č²»“ó£®


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µ„Ī»Ź±¼äĄļĆæŌö¼Ó1molN2£¬Ķ¬Ź±¼õÉŁ2molNH3 | |
| B£® | c£ØN2£©£ŗc£ØH2£©£ŗc£ØNH3£©=1£ŗ1£ŗ1 | |
| C£® | N2ÓėH2µÄĪļÖŹµÄĮæÓėNH3µÄĪļÖŹµÄĮæĻąµČ | |
| D£® | N2”¢H2ŗĶNH3µÄÖŹĮæ·ÖŹż²»ŌŁøıä |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
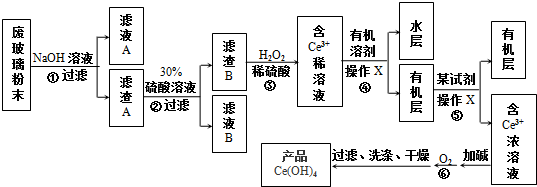
 £¬¶”ĻćÓĶ·Ó²»Ó¦¾ßÓŠµÄ»ÆѧŠŌÖŹŹĒ£Ø””””£©
£¬¶”ĻćÓĶ·Ó²»Ó¦¾ßÓŠµÄ»ÆѧŠŌÖŹŹĒ£Ø””””£©| A£® | æÉŅŌ·¢Éś¼Ó¾Ū·“Ó¦ | B£® | æÉŅŌÓėĒæ¼īČÜŅŗ·“Ó¦ | ||
| C£® | ÓėNaHCO3·“Ó¦·Å³öCO2 | D£® | æÉÓėäåĖ®·¢Éś¼Ó³É·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŹµŃéŠņŗÅ | ²Ł×÷ĻÖĻó |
| i | ȔɣĮæ¹ĢĢåѳʷ£¬¼ÓČė¹żĮæĻ”ŃĪĖį£¬¹ĢĢåČܽā£¬²śÉśĘųĢå£Ø¾¼ģŃéĪŖH2£©£¬ČÜŅŗ³ŹĒ³»ĘÉ« |
| ii | ĻņiĖłµĆČÜŅŗÖŠ¼ÓČėÉŁĮæKSCNČÜŅŗ£¬ČÜŅŗ³ŹĒ³ŗģÉ«£¬ŌŁ¼ÓČėH2O2ČÜŅŗ£¬²śÉśĪŽÉ«ĘųĢå£Ø¾¼ģŃéĪŖO2£¬ČÜŅŗ±äĪŖÉīŗģÉ«£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1molĻ”H2SO4Óė×ćĮæNaOHČÜŅŗ·“Ó¦ | |
| B£® | Ļ”“×ĖįÓėNaOHČÜŅŗ·“Ӧɜ³É1mol H2O | |
| C£® | Ļ”ŃĪĖįÓėĻ”Ba£ØOH£©2ČÜŅŗ·“Ӧɜ³É1mol H2O | |
| D£® | Ļ”NaOHÓė95%ÅØĮņĖį·“Ӧɜ³É1mol H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ×å ÖÜĘŚ | IA | IIA | IIIA | IV A | V A | VI A | VII A | O |
| Ņ» | A | |||||||
| ¶ž | B | C | ||||||
| Čż | D | E | F | G | H | I | ||
| ĖÄ | K | J | ||||||
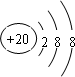 £®
£®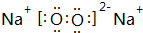 £¬ĖüŹōÓŚĄė×Ó£ØĄė×Ó»ņ¹²¼Ū£©»ÆŗĻĪļ£®
£¬ĖüŹōÓŚĄė×Ó£ØĄė×Ó»ņ¹²¼Ū£©»ÆŗĻĪļ£®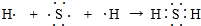 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £Ø²æ·ÖŹŌ¼ĮŗĶ·“Ó¦Ģõ¼žŅŃĀŌČ„£©£®
£Ø²æ·ÖŹŌ¼ĮŗĶ·“Ó¦Ģõ¼žŅŃĀŌČ„£©£®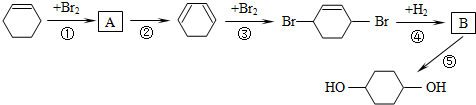
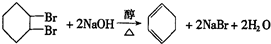
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
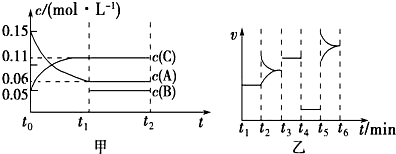
| A£® | Čōt1=15 s£¬t0”«t1½×¶ĪBµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0.004 mol•L-1•s-1 | |
| B£® | t4”«t5½×¶ĪøıäµÄĢõ¼žŹĒ¼õŠ”Ń¹Ēæ | |
| C£® | øĆČŻĘ÷µÄČŻ»żĪŖ2 L£¬BµÄĘšŹ¼ĪļÖŹµÄĮæĪŖ0.02 mol | |
| D£® | t5”«t6½×¶Ī£¬ČŻĘ÷ÄŚAµÄĪļÖŹµÄĮæ¼õÉŁĮĖ0.06 mol£¬ČŻĘ÷ÓėĶā½ēµÄČČ½»»»ĪŖa kJ£¬ŌņøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ3A£Øg£©?B£Øg£©+2C£Øg£©”÷H=-50a kJ•mol-1 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com