
【题目】在一定温度下的定容容器中,当下列哪些物理量不再发生变化时,表明反应A(g)+2B(g) ![]() C(g)+D(g)已达到平衡状态的是
C(g)+D(g)已达到平衡状态的是
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度 ④混合气体总物质的量 ⑤混合气体的平均相对分子质量 ⑥v(C)与v(D)的比值为1:1 ⑦混合气体总质量 ⑧混合气体总体积
A. ①②③④⑤⑥⑦⑧B. ①③④⑤C. ①②③④⑤⑦D. ①③④⑤⑧
【答案】B
【解析】
首先看清条件为恒温恒容,其次是看清反应,该反应是一个正反应方向气体物质的量减少的反应,且反应物、生成物全部为气体。根据平衡状态的判断标志进行判断。
判断化学平衡状态的两种方法
(1)动态标志:v正=v逆≠0
①同种物质:同一物质的生成速率等于消耗速率;
②不同物质:必须标明是“异向”的反应速率关系。如aA+bBcC+dD,![]() 时,反应达到平衡状态。
时,反应达到平衡状态。
(2)静态标志:各种“量”不变
①各物质的质量、物质的量或浓度不变;
②各物质的百分含量(物质的量分数、质量分数等)不变;
③温度、压强(化学反应方程式两边气体体积不相等)或颜色(某组分有颜色)不变;
以及由此衍生的一些物理量也不变,总之,“变化的量”不变了,可作为判断平衡的标志,据此解答。
在一定温度下的定容容器中,反应A(g)+2B(g) ![]() C(g)+D(g)达到平衡状态,正逆反应速率相等,各组分的浓度不再变化,
C(g)+D(g)达到平衡状态,正逆反应速率相等,各组分的浓度不再变化,
①由于反应两边气体的化学计量数之和不相等,气体的物质的量不相等,容器的容积不变,则压强会随着反应进行变化,当混合气体的压强不再发生变化时,说明气体的物质的量不再变化,正逆反应速率相等,达到了平衡状态,①正确;
②根据质量守恒定律知混合气体的总质量不变,容器的容积不变,所以混合气体的密度始终不变,因此混合气体的密度不变无法判断是否达到了平衡状态,②错误;
③B的物质的量浓度不变,说明B的生成速率等于消耗速率,正逆反应速率相等,达到了平衡状态,③正确;
④反应方程式两边气体的体积不相等,气体的物质的量是个变化的量,若混合气体的总物质的量不变,说明达到了平衡状态,④正确;
⑤方程式两边气体的化学计量数之和不相等,气体的物质的量是个变化的量,气体的质量始终不变,混合气体的平均相对分子质量是个变化的量,所以混合气体的平均相对分子质量不变,说明达到了平衡状态,⑤正确;
⑥反应速率比值与化学计量数之比成正比,v(C)与v(D)的比值不变,不能判断是否达到了平衡状态,⑥错误;
⑦反应方程式两边都是气体,根据质量守恒定律知混合气体的总质量不变,所以混合气体的总质量不变,无法判断是否达到了平衡状态,⑦错误;
⑧容器的容积不变,混合气体的体积始终不变,所以混合气体的总体积不变,无法判断是否达到了平衡状态,⑧错误;
综上所述①③④⑤均能判断反应已达到平衡状态;
答案选B。


科目:高中化学 来源: 题型:
【题目】如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法错误的是

A. 该反应的热化学方程式为:N2(g)+O2(g)═2NO(g)△H=+180kJ·mol﹣1
B. 1mol N2(l)和NA个O2(l)反应生成2mol NO(g)时,吸收的能量为180kJ
C. 1mol N2(g)和1mol O2(g)具有的总能量小于2mol NO(g)具有的总能量
D. 通常情况下,N2(g)和O2(g)混合不能直接生成NO(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图象分别表示有关反应的反应过能量变化的关系:据此判断下列说法中正确的是( )
A. 石墨转变为金刚石是吸热反应
B. 白磷比红磷稳定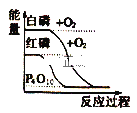
C. (g)+O2(g)=SO2(g) △H1 S(s)+O2(g)=SO2(g) △H2,则△H1>△H2
D. CO(g)+H2O(g)=CO2(g)+H2(g) △H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究甲醛与新制的Cu(OH)2的反应:
(1)向6 mL 6 mol·L1 NaOH溶液中滴加8滴2%CuSO4溶液,振荡,加入0.5 mL15%甲醛溶液,混合均匀,水浴加热,迅速产生红色沉淀,其周围剧烈产生无色气体。
(2)反应停止后分离出沉淀,将所得沉淀洗净后加入浓盐酸,不溶解。
(3)相同条件下,甲酸钠溶液与新制的Cu(OH)2反应,未观察到明显现象。
已知:Cu2O![]() [CuCl2],甲醛是具有强还原性的气体。
[CuCl2],甲醛是具有强还原性的气体。
下列说法正确的是
A.红色沉淀的主要成分不是Cu2O,可能是Cu
B.将产生的无色气体通过灼热的CuO后得到红色固体,气体中一定含有CO
C.从甲醛的结构 ![]() 推测,其氧化产物可能为碳酸(
推测,其氧化产物可能为碳酸(![]() ),因此实验中得到的无色气体是CO2
),因此实验中得到的无色气体是CO2
D.含有-CHO的有机物都可以被新制Cu(OH)2氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式书写正确的是
A. 2SO2 + O2![]() 2SO3 △H=-196.6 kJ·mol-1
2SO3 △H=-196.6 kJ·mol-1
B. C(s) + O2(g) = CO2(g) △H=393.5 kJ·mol-1
C. H+(aq) + OH-(aq) = H2O(l) △H=57.3 kJ
D. ![]() H2(g) +
H2(g) + ![]() Cl2(g) = HCl(g) △H=-92.5 kJ·mol-1
Cl2(g) = HCl(g) △H=-92.5 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,质量相同的CO2、H2、O2、CH4、SO2五种气体,下列说法错误的是( )
A.所占的体积由大到小的顺序是:H2>CH4>O2>CO2>SO2
B.所含的质子数由多到少是:CO2>SO2>CH4>O2>H2
C.密度由大到小的顺序是:SO2>CO2>O2>CH4>H2
D.所含分子数由多到少的顺序是:H2>CH4>O2>CO2>SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组设计的简易原电池装置如下图所示。该电池工作时,下列说法不正确的是
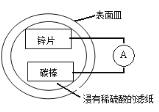
A.锌片作负极
B.碳棒上有气泡产生
C.电子由锌片经导线流向碳棒
D.可将电能转化为化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《神农本草经》记载,神农尝百草,日遇七十二毒,得茶而解。茶叶中铁元素的检验可经以下四个步骤完成,各步骤中选用的实验用品不能都用到的是( )
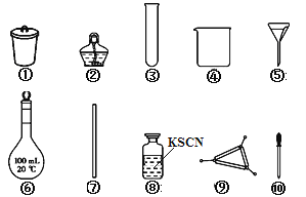
A. 将茶叶灼烧灰化,选用①、②和⑨
B. 用浓盐酸溶解茶叶灰并加蒸馏水稀释,选用④、⑥和⑦
C. 过滤得到滤液,选用④、⑤和⑦
D. 检验滤液中的Fe3+,选用③、⑧和⑩
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气体A是一种三原子分子,某学习小组按下列流程进行了实验:
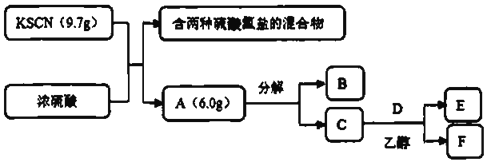
其中,将金属钠投入足量的无水乙醇,往反应液中通人![]() ,可制得D,C和D按
,可制得D,C和D按![]() 反应生成等物质的量的E和F.已知:B是一种常见的氧化物;C是一种淡黄色的固体单质;E在标准状况下的密度约为
反应生成等物质的量的E和F.已知:B是一种常见的氧化物;C是一种淡黄色的固体单质;E在标准状况下的密度约为![]() 。请回答:
。请回答:
(1)A的结构_______________,其空间构型为_______________。
(2)KSCN粉末与浓硫酸反应生成A的化学方程式_________________;为检验硫酸氢盐混合物中的![]() ,请写出实验操作和现象______________________________。
,请写出实验操作和现象______________________________。
(3)A不太稳定,容易分解,写出A分解为B和C的化学方程式________________________。
(4)①D的化学式________________。
②F的成键情况与![]() 相似,F的电子式________________。
相似,F的电子式________________。
③工业上常用电解熔融NaCl制Na,事实上电解许多熔融的钠的化合物也能制备Na,如NaOH.试写出电解熔融NaOH的化学方程:________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com