
| A.干电池 | B.光伏电池 | C.离子交换膜电解槽 | D.风力发电机 |
科目:高中化学 来源:不详 题型:填空题
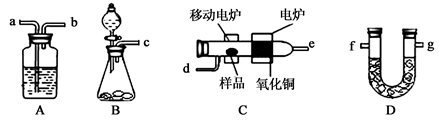
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
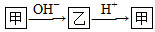 。请回答下列问题:
。请回答下列问题:
 H2NCOONH4(l)(氨基甲酸铵) ΔH1
H2NCOONH4(l)(氨基甲酸铵) ΔH1 H2O(l)+H2NCONH2(l)(尿素) ΔH2
H2O(l)+H2NCONH2(l)(尿素) ΔH2
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.由图可知,该反应为放热反应 |
| B.该反应的焓变为ΔH=-(E2-E1) |
| C.曲线b相对曲线a来说,改变的条件只能是使用了催化剂 |
| D.该反应的发生条件一定是加热 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③⑤ | B.①②③⑦ |
| C.①②⑤⑥⑦ | D.④⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.过程Ⅰ是吸热过程 |
| B.过程Ⅲ一定是放热过程 |
| C.该反应过程所有旧化学键都断裂,且形成了新化学键 |
| D.该反应的能量转化形式只能以热能的形式进行 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

A.该反应的热化学方程式为:2NH3  N2+3H2ΔH =-92 kJ·mol-1 N2+3H2ΔH =-92 kJ·mol-1 |
| B.正反应的活化能小于逆反应的活化能 |
| C.a曲线是加入催化剂时的能量变化曲线 |
| D.加入催化剂可增大正反应速率,降低逆反应速率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①④ | B.①②③ | C.④⑤⑥ | D.①④⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com