
 过渡金属元素氧化物的应用研究是目前科学研究的前沿之一,试回答下列问题:
过渡金属元素氧化物的应用研究是目前科学研究的前沿之一,试回答下列问题:| 1 |
| 8 |
| 1 |
| 2 |
|
| 1-x |
| x |
| 1-x |
| x |


科目:高中化学 来源: 题型:
| A、原子半径:Y>Z>W |
| B、非金属性最强的元素为W |
| C、Y的最高价氧化物对应的水化物为强碱 |
| D、XW2分子中各原子最外层电子未达到8电子结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10 与 19 |
| B、6 与 16 |
| C、11 与 17 |
| D、14 与 8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
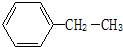
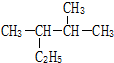
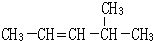
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验步骤(不要求写具体操作过程) | 预期现象和结论 |
| ①测定甲同学所用Fe(N3O)3溶液的pH ② … |
若银镜消失,假设2成立.若银镜不消失,假设2不成立. |
查看答案和解析>>
科目:高中化学 来源: 题型:
 按要求问答下列问题
按要求问答下列问题查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
| 太阳光 |

| n(CH3OH) |
| n(CO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、滴加甲基橙试液显红色的溶液:Fe2+、NH4+、SCN-、ClO- |
| B、含有大量SO42-的溶液:NH4+、Mg2+、Cl-、NO3- |
| C、水电离出的c(H+)=1×10-12 mol/L的溶液:S2O32-、C2O42-、K+、Na+ |
| D、能与Al反应放出H2的溶液:K+、Na+、NO3-、SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com