

 ;
; ,F发生酯化反应生成G,则F为
,F发生酯化反应生成G,则F为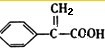 ,根据碳链结构可知A为
,根据碳链结构可知A为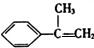 ,A发生加成反应生成B,B为
,A发生加成反应生成B,B为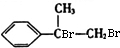 ,B发生取代反应生成C,C为
,B发生取代反应生成C,C为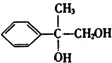 ,C发生氧化反应生成D,D为
,C发生氧化反应生成D,D为 ,D发生氧化反应生成E,E为
,D发生氧化反应生成E,E为 ,E发生缩聚反应生成H,H为
,E发生缩聚反应生成H,H为 ,据此分析解答.
,据此分析解答. ;
; ,F发生酯化反应生成G,则F为
,F发生酯化反应生成G,则F为 ,根据碳链结构可知A为
,根据碳链结构可知A为 ,A发生加成反应生成B,B为
,A发生加成反应生成B,B为 ,B发生取代反应生成C,C为
,B发生取代反应生成C,C为 ,C发生氧化反应生成D,D为
,C发生氧化反应生成D,D为 ,D发生氧化反应生成E,E为
,D发生氧化反应生成E,E为 ,E发生缩聚反应生成H,H为
,E发生缩聚反应生成H,H为 ,
, ,故答案为:
,故答案为: ;
; ,化合物E中的官能团有羟基、羧基,故答案为:羟基、羧基;
,化合物E中的官能团有羟基、羧基,故答案为:羟基、羧基; ,发生催化氧化生成
,发生催化氧化生成 ,反应的方程式为
,反应的方程式为 ;
; 、E为
、E为 ,E发生消去反应生成F,反应方程式为
,E发生消去反应生成F,反应方程式为
| 浓H2SO4 |
| △ |
 +H2O,
+H2O, ;
;
| 浓H2SO4 |
| △ |
 +H2O;
+H2O; ,E的同分异构体符合下列条件:
,E的同分异构体符合下列条件: 、
、 ,
, 、
、 .
.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
| A、常温常压下,17g羟基中所含电子数为9NA |
| B、常温下,1 molFe与足量浓硝酸反应,转移2 NA个电子 |
| C、常温常压下,22.4L的NO2和CO2混合气体含有2 NA个O 原子 |
| D、在0.1 mol过氧化钠中,阴离子总数等于0.2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子半径:W>X>Z |
| B、原子半径:Z>X>Y |
| C、单质的熔点:W>Z>Y |
| D、最高正价:Z>W>X |
查看答案和解析>>
科目:高中化学 来源: 题型:


 ,该物质在NaOH水溶液中加热反应,可生成有机物的结构简式为
,该物质在NaOH水溶液中加热反应,可生成有机物的结构简式为 的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:CH2=CH2
的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:CH2=CH2| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol[Zn(NH3)4]Cl2中含有σ键的数目为16NA |
| B、电解精炼粗铜时,每转移NA电子,阳极上溶解的铜原子数必为0.5NA |
| C、3.0 g淀粉和葡萄糖混合物中共含碳原子数为0.1NA |
| D、60 g石英晶体中含有的Si-O键数目为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com