
| A. | 2 L 0.1 mol•L-1的AlCl3溶液 | B. | 1 L 0.1 mol•L-1的FeCl2溶液 | ||
| C. | 1 L 1 mol•L-1的NaCl溶液 | D. | 1 L 2 mol•L-1的KClO3溶液 |
分析 根据溶液中不水解的离子的物质的量浓度=溶质的物质的量浓度×化学式中离子的个数,与溶液的体积无关,据此分析解答.
解答 解:A.2 L 0.1 mol•L-1的AlCl3溶液,氯离子浓度为0.1mol/L×3=0.3mol/L;
B.1 L 0.1 mol•L-1的FeCl2溶液,氯离子浓度为0.1mol/L×2=0.2mol/L;
C.1 L 1 mol•L-1的NaCl溶液,氯离子浓度为1mol/L×1=1mol/L;
D.氯酸钾溶液中不含有氯离子;
Cl-的浓度最大的是1mol/L,
故选:C.
点评 本题考查物质的量浓度的计算与理解,题目难度不大,注意溶液中溶质离子的浓度与溶液体积无关,只取决于物质电离出的离子的数目多少与溶质的浓度.


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:多选题
| A. | 将CO2溶于水中 | B. | Na2O2溶于水中 | C. | 将SO3溶于水中 | D. | NaHSO4溶于水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ②④ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | Na+ | H+ | Ba2+ |
| 阴离子 | OH- | CO32- | SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
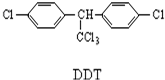
| A. | 它属于芳香烃 | B. | 分子式为C14H8Cl5 | ||
| C. | 1mol该物质能与6mol H2加成 | D. | 分子中最多可能有28个原子共面 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | 沸点/℃ | 熔点/℃ | 密度(20℃)/g•cm-3 | 溶解性 |
| 甲醇 | 64.7 | / | 0.7915 | 易溶于水 |
| 乙醚 | 34.5 | / | 0.7138 | 微溶于水 |
| 3,5-二甲氧基苯酚 | / | 33-36 | / | 易溶于甲醇、乙醚,微溶于水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com