
科目:高中化学 来源: 题型:
 如图所示装置中,X和Y均为石墨电极.
如图所示装置中,X和Y均为石墨电极.
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
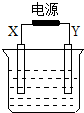 如图,X和Y均为石墨电极:
如图,X和Y均为石墨电极:查看答案和解析>>
科目:高中化学 来源: 题型:022
已知铅蓄电池放电时的电极反应:
负极:Pb+SO42-=PbSO4+2e-
正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O
若用此电池(惰性电极)电解饱和食盐水,当阴、阳两极收集到的气体总体积为1.68L(标准状况)时,该蓄电池内消耗H2SO4______。
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:022
负极:Pb+SO42-=PbSO4+2e-
正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O
若用此电池(惰性电极)电解饱和食盐水,当阴、阳两极收集到的气体总体积为1.68L(标准状况)时,该蓄电池内消耗H2SO4______。
查看答案和解析>>
科目:高中化学 来源: 题型:
(10分)如图,X和Y均为石墨电极:
(1)若电解液为滴有酚酞的饱和食盐水,
电解反应的离子方程式为:
电解过程中 极(填阴或阳)附近会出现红色;
 (2)若电解液为500mL含A溶质的某蓝色溶液,电解一段时间,观察到x电极表面有红色固态物质生成,Y电极有无色气体生成;当溶液中原有溶质完全电解后,取出x电极,洗涤、干燥、称量,电极增重1.6g。
(2)若电解液为500mL含A溶质的某蓝色溶液,电解一段时间,观察到x电极表面有红色固态物质生成,Y电极有无色气体生成;当溶液中原有溶质完全电解后,取出x电极,洗涤、干燥、称量,电极增重1.6g。
①电解后溶液的pH= ;要使电解后溶液恢复到电解前的状态,需加入一定量的
(填物质的化学式)(假设电解前后溶液的体积不变)。
②请你推测原溶液中所含的酸根离子可能是 ;并设计实验验证你的推测,写出实验的操作步骤、现象和结论
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com