
可逆反应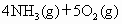
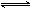
 ,该反应在10L的密闭容器中进行,30s后,水蒸气的物质的量增加了0.45mol,请分别用
,该反应在10L的密闭容器中进行,30s后,水蒸气的物质的量增加了0.45mol,请分别用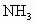 、
、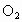 、NO、
、NO、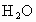 表示该可逆反应的化学反应速率.
表示该可逆反应的化学反应速率.
科目:高中化学 来源: 题型:
 已知可逆反应:FeO(s)+CO(g)
已知可逆反应:FeO(s)+CO(g) Fe(s)+CO2(g)是炼铁工业中的一个重要反应,其温度T与n(CO2)/n(CO)的比值关系如右下表所示.下列有关说法正确的是( )
Fe(s)+CO2(g)是炼铁工业中的一个重要反应,其温度T与n(CO2)/n(CO)的比值关系如右下表所示.下列有关说法正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

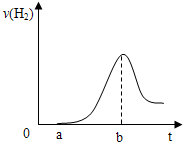
查看答案和解析>>
科目:高中化学 来源: 题型:
 可逆反应Fe(s)+CO2(g)?FeO(s)+CO(g),在温度938K时,平衡常数K=1.47,在1173K时,K=2.15
可逆反应Fe(s)+CO2(g)?FeO(s)+CO(g),在温度938K时,平衡常数K=1.47,在1173K时,K=2.15| C(CO) |
| C(CO2) |
| C(CO) |
| C(CO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
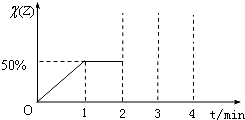
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com