
һ�������´��ڷ�Ӧ��H2��g��+I2��g��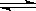 2HI��g����H<0������������ͬ��1L���ݾ��ȣ������û�������������ܱ��������ڢ��г���1molH2��1molI2��g�����ڢ��г���2molHI��g�����ڢ��г���2molH2��2molI2��g����700�������¿�ʼ��Ӧ���ﵽƽ��ʱ������˵����ȷ����
2HI��g����H<0������������ͬ��1L���ݾ��ȣ������û�������������ܱ��������ڢ��г���1molH2��1molI2��g�����ڢ��г���2molHI��g�����ڢ��г���2molH2��2molI2��g����700�������¿�ʼ��Ӧ���ﵽƽ��ʱ������˵����ȷ����
A��������������Ӧ������ͬ
B���������з�Ӧ��ƽ�ⳣ�������������з�Ӧ��ƽ�ⳣ��
C���������е�������ɫ���������е�������ɫ��
D����������H2��ת��������������HI��ת����֮�͵���1

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017�����ɹŸ����ϵڶ����¿���ѧ�Ծ��������棩 ���ͣ�ʵ����
��.���ú��̷�ˮ����Ҫ��Mn2+��SO42-��H����Fe2+��Al3����Cu2+�����Ʊ������ܴ��Բ���̼���̣�MnCO3��������һ�ֹ����������£�

��֪ijЩ������ȫ������pH���±���
������ | Fe��OH��3 | Al��OH��3 | Cu��OH��2 | Mn��OH��2 | CuS | MnS | MnCO3 |
������ȫʱ��pH | 3.2 | 5.4 | 6.4 | 9.8[ | ��0 | ��7 | ��7 |
�ش� �������⣺
�������⣺
��1�����̢��У���������W����Ҫ�ɷ��� ��
��2�����̢��У�������Ӧ�����ӷ���ʽ�� ��
��3�����̢��У������ɵ�����J��ʹ����ʯ��ˮ����ǣ�������MnCO3�ķ�Ӧ�����ӷ���
ʽ�� ��
��4����MnCO3���Ƶ���Ҫ�Ĵ���MnO2��2MnCO3��O2=2MnO2��2CO2�����ڿ����м���460.0 g MnCO3���õ�332.0 g��Ʒ������Ʒ������ֻ��MnO����ò�Ʒ��MnO2������������ ���ðٷ�����ʾ��С�������1λС������
��.�����£�Ũ�Ⱦ�Ϊ0.1 mol��L��1������������Һ��pH���±���
���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
��1����������Һ�е������ӣ����H��������ǿ���� ��
��2�����ݱ��������жϣ�Ũ�Ⱦ�Ϊ0.01 mol��L��1���������ʵ���Һ�У�������ǿ���� ������ţ���
A��HCN
B��HClO
C��C6H5OH
D�� CH3COOH
CH3COOH
E��H2CO3
��3�������ϱ����ݣ������ж����з�Ӧ���ܳ������� ������ţ���
A��HCN��Na2CO3=NaHCO3�� NaCN
NaCN
B��CH3COOH��NaCN=CH3COONa��HCN
C��CO2��H2O��2C6H5ONa=Na2CO3��2C6H5OH
D��CH3COONa��HClO=NaClO��CH3COOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�캣��ʡ������10���¿���ѧ�Ծ��������棩 ���ͣ��ƶ���
I������ѡ����
�Ǽ��㶹����һ�ּ���Ⱦ�ϣ�Ӧ���ڿɵ�гȾ�ϼ��������Ǽ��㶹�ط���ģ����ͼ��ʾ�����й������������
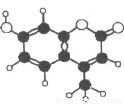
A������ʽΪC10H9O3
B��������ˮ����ȡ����Ӧ�ͼӳɷ�Ӧ����Ũ���������²��ܷ�����ȥ��Ӧ
C����ʹ���Ը��������Һ��ɫ
D��1mol�Ǽ��㶹���������2molNaOH��1mol�Ǽ��㶹���������4 mol H2�����ӳɷ�Ӧ
������A�Ǻϳ���Ȼ�ĵ��壬����ʽΪC5H8��A��һϵ�з�Ӧ����(���ַ�Ӧ������ȥ����
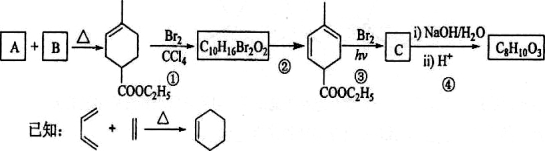
�ش��������⣺
��1��A�Ļ�ѧ������ ��
��2��B�ķ���ʽΪ ��
��3���ڵķ�Ӧ����ʽΪ ��
��4���ٺ͢۵ķ�Ӧ���ͷֱ��� ��
��5��CΪ�������������������Ǽ����ܵ�i����ѧ����ʽΪ ��
��6��A��ͬ���칹���в����ۼ�˫ϩ(C=C=C���ṹ��Ԫ����״������ �֣����������칹�壩��д�����л�Ϊ�����칹 ��Ļ�����Ľṹ��ʽ ��
��Ļ�����Ľṹ��ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�캣��ʡ������10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
������ϩ���������������³�Ա����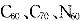 ֮��������ѧ���״η�����ȫ����ϩ
֮��������ѧ���״η�����ȫ����ϩ ������˵����ȷ����
������˵����ȷ����
A B40��C70���������ͻ�����
B C60��N60����ͬ���칹��
C��B40��C60��N60��C70��ֻ�����ۼ�
D��B40��C60��N60��C70������ϩ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�߶������л�ѧ���������棩 ���ͣ�ѡ����
��ӦA2+B2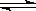 2AB�ڲ�ͬ�����£�����AB�ٷֺ�����ʱ��仯��ϵ��ͼ��ʾ��aΪ500�棬bΪ300��ʱ�����cΪ300��ʱ��ʱ��t3��ʼ�������м�ѹ�������������������ȷ����
2AB�ڲ�ͬ�����£�����AB�ٷֺ�����ʱ��仯��ϵ��ͼ��ʾ��aΪ500�棬bΪ300��ʱ�����cΪ300��ʱ��ʱ��t3��ʼ�������м�ѹ�������������������ȷ����
A��A2��B2��AB��Ϊ���壬����Ӧ����
B��ABΪ����,A2��B2��������һ��Ϊ�����壬����Ӧ����
C��ABΪ����,A2��B2��������һ��Ϊ�����壬����Ӧ����
D��ABΪ����,A2��B2��������һ��Ϊ�����壬����Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�߶������л�ѧ���������棩 ���ͣ�ѡ����
���CuSO4��Һʱ����Ҫ�ﵽ��������Ҫ�������������٣��������������ӣ�����Һ��c��Cu2+�����䡣��ѡ�õĵ缫��
A����ͭ����������Zn��Ag��ͭ�Ͻ�������
B����Zn��Ag��ͭ�Ͻ�����������ͭ������
C���ô������������ô�ͭ������
D����ʯī���������ö��Ե缫��Pt��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�߶������л�ѧ���������棩 ���ͣ������
����A��B��C��D��E������Һ�ֱ������ᡢ���ᡢ����������Һ����ˮ��̼������Һ�е�һ�֡������½�������ʵ�飺
��� | ʵ�鲽��ͽ��� |
�� | �Ƚ�Ũ�Ⱦ�Ϊ0.1 mol��L��1��A��E��pH�Ĵ�СΪ��7��A��E |
�� | 1 L pH��9��A�ֱ���xL 0.001mol��L-1 B��yL 0.001mol��L-1 D��ַ�Ӧ����Һ��������ʱx��y�Ĵ�С��ϵΪ��y<x�� |
�� | pH��a��C��pH��b��D����a+b=14,�������Ϸ�������кͷ�Ӧ����Һ�ʼ��ԡ� |
��1��A��������___________�� D��������___________��E��������___________�����ѧʽ��
��2����������������ʵ���Ũ�ȵ�D��E�ֱ������������۷�Ӧ����ͬ�����²������������֮��Ϊ _______________��
��3����������������ʵ���Ũ�ȵ�B��C��Ϻ�������Һ��PHΪ7���ּ�֪���������ǿ��̼�ᣬ�ɴ˿��ƶ�̼�����ˮ��Һ��___________����ᡱ��������С����ԡ�
��4����D��Һ��εμӵ�A��Һ�У��������D�����ʵ�����A���ʱ����Һ�����������ӵ����ʵ���Ũ���ɴ�С�Ĺ�ϵΪ____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�߶������л�ѧ���������棩 ���ͣ�ѡ����
�ں��¡���ѹ�£�a mol A��b mol B��һ���ݻ��ɱ�������з�����Ӧ��A��g����2B��g��  2C��g����һ��ʱ���ﵽƽ�⣬����n mol C��������˵������ȷ����
2C��g����һ��ʱ���ﵽƽ�⣬����n mol C��������˵������ȷ����
A������A��B��ת����֮��Ϊa��b
B����ʼʱ�̺ʹ�ƽ��������е�ѹǿ֮��Ϊ��a+b���ã�a+b-n/2��
C������ʼʱ����2 a mol A��2b mol B����ﵽƽ��ʱ����2nmol C
D����2V����A����2V�棨B�� ʱ����֤����Ӧ�ﵽƽ��״̬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��ӱ�ʡ�߶������л�ѧ���������棩 ���ͣ�ѡ����
��֪ij�¶���CH3COOH��NH3•H2O �ĵ��볣����ȣ�����10mLŨ��Ϊ0.1mol•L?1��CH3COOH��Һ�еμ���ͬŨ�ȵİ�ˮ���ڵμӹ�����
A��ˮ�ĵ���̶�ʼ������
B�� �������ټ�С
�������ټ�С
C��c��CH3COOH����c��CH3COO?��֮��ʼ�ձ��ֲ���
D�������백ˮ�����Ϊ10mLʱ��c��NH4+��=c��CH3COO? ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com