
| 78.4 |
| 22.4 |
| 120 |
| 80 |
| 78.4 |
| 22.4 |
| 120 |
| 80 |
| 1.5 |
| 2 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��CH3CH=CH2+Br2
| |||
B��CH3CH2OH
| |||
C��CH3COOH+CH3CH2OH
| |||
D��2CH3CH2OH+O2
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��4NO2��g��+O2��g��=2N2O5��g������H��0 |
| B��2CO��g��=2C��s��+O2��g������H��0 |
| C����NH4��2CO3��s��=NH4HCO3��s��+NH3��g������H��0 |
| D��2H2��g��+O2��g��=2H2O��l������H��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����״���£�1 mol�κ����������ԼΪ22.4 L |
| B��ͬ�¡�ͬѹ�£������ͬ���������嵥�ʾ�����ͬ�ķ�����Ŀ |
| C����73 g HCl����1 Lˮ�������Һ��������Һ���ʵ���Ũ����2 mol?L-1 |
| D����NA��Na+��Na2O�ܽ���ˮ���1 L��Һ��Na+�����ʵ���Ũ��Ϊ1 mol?L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
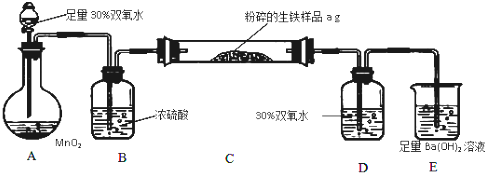
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ZΪ0.3mol/L |
| B��Y2Ϊ0.4mol/L |
| C��X2Ϊ0.2mol/L |
| D��ZΪ0.4mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com