
【题目】下列关于NH4+、NH3、NH2﹣三种微粒的说法不正确的是( )
A.三种微粒所含有的电子数相等
B.三种微粒中氮原子的杂化方式相同
C.三种微粒的空间构型相同
D.键角大小关系:NH4+>NH3>NH2﹣
【答案】C
【解析】解:A.NH4+、NH3、NH2﹣三种微粒,每个NH4+、NH3、NH2﹣所含有的电子数都为10个电子,故A正确; B.铵根离子中氮原子价层电子对个数=σ键个数+孤电子对个数=4+ ![]() =4,所以其采用sp3杂化,氨气分子中价层电子对个数=σ键个数+孤电子对个数=3+
=4,所以其采用sp3杂化,氨气分子中价层电子对个数=σ键个数+孤电子对个数=3+ ![]() (5﹣3×1)=4,所以氮原子杂化方式是sp3 , NH2﹣中氮原子价层电子对个数=σ键个数+孤电子对个数=2+
(5﹣3×1)=4,所以氮原子杂化方式是sp3 , NH2﹣中氮原子价层电子对个数=σ键个数+孤电子对个数=2+ ![]() =4,所以其采用sp3杂化,故B正确;
=4,所以其采用sp3杂化,故B正确;
C.铵根离子为正四面体结构;氨气分子空间构型为三角锥形,NH2﹣空间构型为V形,故C错误;
D.铵根离子中,含0对孤电子,氨气分子中含1对孤电子,NH2﹣含2对孤电子,含有孤电子对越多,分子中的键角越小,所以键角大小关系:NH4+>NH3>NH2﹣ , 故D正确;
故选C.


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
【题目】柠檬烯是一种食用香料,结构简式如图,有关柠檬烯的分析正确的是( ) ![]()
A.柠檬烯的一氯代物有8种
B.柠檬烯和 ![]() 互为同分异构体
互为同分异构体
C.柠檬烯的分子中所有的碳原子可能在同一个平面上
D.一定条件下,柠檬烯可以发生加成、取代、氧化、加聚、酯化等反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸与合成氨工业密切相关,氨氧化法是工业生产中制取硝酸的主要途径.完成下列计算:
(1)合成氨时,假设100L的氮气与氢气(体积比为1:3)的混合气体通过氨合成塔充分反应后,体积变为90L,则氮气的转化率为 . (写出计算过程,计算结果请用百分数表示)
(2)标准状况下,将500L氨气溶于1L水中形成氨水,则此氨水质量分数为 . (写出计算过程,计算结果请用百分数表示,并保留1位小数)
(3)氨氧化法是将氨和空气的混合气通过灼热的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮(NO).此时温度很高,水以水蒸气的形式存在,NO也不与O2反应.若氨气与氧气物质的量之比为1:1.7时,氨的转化率可达95%,计算反应后NO的体积分数 . (设氧气在空气中的体积分数为20%,写出计算过程,计算结果请用百分数表示并保留1位小数)
(4)一氧化氮继续氧化为二氧化氮,二氧化氮溶于水可得硝酸.为测定某18K金样品的组成,将2.832g样品粉碎后投入足量的浓硝酸中,充分溶解后,收集到NO2和N2O4的混合气体224mL(折算至标准状况,下同),将该混合气体与84mL O2混合后缓缓通入水中,恰好被完全吸收.( 已知金不溶于浓硝酸) 填写该18K金的成分表(写出计算过程,计算结果请用百分数表示并保留1位小数,若不含该金属则填0).
18K金成分 | Au | Ag | Cu |
含量(质量分数) | 75% |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学反应原理分析解答以下问题:
(1)弱酸在水溶液中存在电离平衡,部分0.1molL﹣1弱酸的电离平衡常数如下表:
弱酸 | 电离平衡常数(25℃) |
HClO | K=2.98×10﹣8 |
H2CO3 | K1=4.3×10﹣7 |
H2SO3 | K1=1.54×10﹣2 |
①当弱酸的浓度一定时,降低温度,K值(填“变大”“变小”或“不变”).
②下列离子方程式和有关说法错误的是 .
a.少量的CO2通入次氯酸钠溶液中:2ClO﹣+H2O+CO2═2HClO+CO32﹣
b.少量的SO2通入碳酸钠溶液中:SO2+H2O+2CO32﹣═2HCO3﹣+SO32﹣
c.相同温度时,等物质的量浓度的三种弱酸与足量NaOH溶液完全中和消耗NaOH的体积为V(H2CO3)>V(H2SO3)>V(HClO)
d.相同温度时,等pH三种盐溶液的物质的量浓度关系:c(Na2CO3)<c(NaClO)<c(Na2SO3)
③亚硒酸(H2SeO3)也是一种二元弱酸,有较强的氧化性.往亚硒酸溶液中不断通入SO2会产生红褐色单质,写出该反应的化学方程式: .
(2)工业废水中常含有一定量的Cr2O72﹣和CrO42﹣ , 它们对人类及生态系统会产生很大损害,必须进行处理后方可排放. ①在废水中存在平衡:2CrO42﹣(黄色)+2H+Cr2O72﹣(橙色)+H2O.若改变条件使上述平衡向逆反应方向移动,则下列说法正确的是 .
a.平衡常数K值可以不改变
b.达到新平衡CrO42﹣的消耗速率等于Cr2O72﹣的消耗速率
c.达到新平衡后,溶液pH一定增大
d.再达平衡前逆反应速率一定大于正反应速率
②Cr2O72﹣和CrO42﹣最终生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)Cr3+(aq)+3OH﹣(aq),常温下Cr(OH)3的Ksp=10﹣32 , 当c(Cr3+)降至10﹣3 molL﹣1 , 溶液的pH调至4时,(填“有”或“没有”)沉淀产生.
(3)已知:①2CH3OH(g)CH3OCH3(g)+H2O(g) ②CO(g)+2H2(g)CH3OH(g)
③CO(g)+H2O(g) CO2(g)+H2(g)
某温度下三个反应的平衡常数的值依次为K1、K2、K3 , 则该温度下反应3CO(g)+3H2(g)CH3OCH3(g)+CO2(g)的化学平衡常数K=(用含K1、K2、K3的代数式表示).向某固定体积的密闭容器中加入3mol CO和3mol H2 , 充分反应后恢复至原温度,测定容器的压强为反应前的 ![]() ,则CO的转化率为 .
,则CO的转化率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B两种有机物的分子式相同,都可用CaHbOcNd表示,且a+c=b,a-c=d。已知A是天然蛋白质水解的最终产物;B是一种含有醛基的硝酸酯。试回答:
(1)A和B的分子式是________________。
(2)光谱测定显示,A的分子结构中不存在甲基,则A的结构简式为_______________________。
(3)光谱测定显示,B的烃基中没有支链,则B的结构简式为_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一个石墨作电极,电解稀的Na2SO4溶液的装置,通电后在石墨电极A和B附近分别滴加一滴石蕊溶液.下列有关叙述正确的是( ) 
A.逸出气体的体积,A电极的小于B电极的
B.一电极逸出无味气体,另一电极逸出刺激性气味气体
C.A电极附近呈红色,B电极附近呈蓝色
D.电解一段时间后,将全部电解液转移到同一烧杯中,充分搅拌后溶解呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X-的核外电子排布为2、8、8,则X元素在周期表中的位置是( )
A.第三周期第0族B.第四周期第ⅠA族
C.第三周期第ⅠA族D.第三周期第ⅦA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一种有机物,通过元素分析得到的数据为C:85.71%,H:14.29%(质量分数).质谱数据表明它的相对分子质量为84.已知该物质可能存在多种结构,A、B和C是其中的三种.请根据下列要求填空:
(1)该化合物的分子式为;
(2)A与氢气加成生成2﹣甲基戊烷,则A的结构可能有种(考虑顺反异构);
(3)经检验B不能使酸性高锰酸钾溶液褪色,且一氯代物只有两种,则B的结构简式为
(4)已知烯烃能发生反应: ![]()
C经臭氧化并经锌和水处理生成D和E,如图: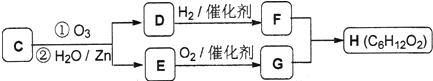
己知D常温为气体,H核磁共振氢谱显示有两组峰,峰面积之比为3:1.
①物质C的名称:;
②E与银氨溶液反应的化学方程式为:;
③F与G生成H的化学方程式为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、G、H、I、J是中学化学常见的9种化合物,F、H常温下呈气态,B常温下呈液态,其中F是人类生存不能离开的气体单质,反应③常用于焊接和切割金属,其转化关系如下图,据此回答下列问题:
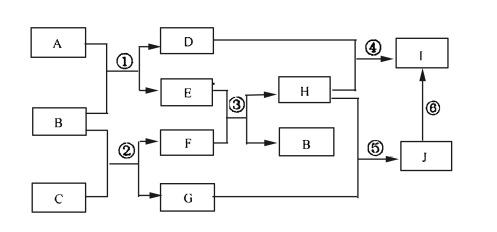
(1)写出C的电子式__________________。
(2)写出反应①的化学方程式______________________。
(3)列出两种E能发生的反应类型_________________________。
(4)写出过量的H与D溶液反应的离子方程式________________。
(5)实验室制取H的装置可以选用下列装置中的(填下图中的选项字母)。
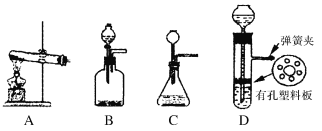
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com