
下列与化学反应能量变化相关的叙述正确的是()
A. 生成物总能量一定低于反应物总能量
B. 放热反应的反应速率总是大于吸热反应的反应速率
C. 应用盖斯定律,可计算某些难以直接测量的反应焓变
D. 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同
考点: 化学反应中能量转化的原因;吸热反应和放热反应;反应热和焓变;用盖斯定律进行有关反应热的计算.
分析: 化学反应中一定伴随着能量变化,反应中既有放热反应,又有吸热反应,取决于反应物和生成物总能量的大小,生成物的总能量低于反应总能量的反应,是放热反应,若是吸热反应则相反,化学反应速率取决于物质的性质和外界反应条件,与反应是吸热还是放热没有必然的联系,反应热只取决于反应物和生成物总能量的大小,与反应条件无关.
解答: 解:A、生成物的总能量低于反应总能量的反应,是放热反应,若是吸热反应则相反,故A错;
B、反应速率与反应是吸热还是放热没有必然的联系,故B错;
C、化学反应的反应热大小取决于反应物和生成物的总能量大小,与反应途径无关,应用盖斯定律,可计算某些难以直接测量的反应焓变,故C正确;
D、根据△H=生成物的焓﹣反应物的焓可知,焓变与反应条件无关,在光照和点燃条件下该反应的△H相同,故D错.
故选:C.
点评: 本题考查化学反应中能量的变化,着重于对概念的理解,注意放热反应、吸热反应与反应物、生成物以及反应速率、反应条件之间有无必然关系,做题时不要混淆.


科目:高中化学 来源:2014-2015学年河北省高三下学期期中考试理综化学试卷(解析版) 题型:选择题
下列实验所用试剂、现象和结论均正确的是
实验序号 | 实验内容 | 试剂 | 现象和结论 |
① | 鉴别K2CO3和Na2SO3 | 盐酸、澄清的石灰水 | 产生无色无味气体,能使澄清的石灰水变浑浊的是K2CO3 |
② | 鉴别NO2 和Br2蒸气 | 湿润的淀粉KI试纸 | 试纸变蓝色的是Br2 |
③ | 鉴别葡萄糖和蔗糖 | 银氨溶液 | 有银镜产生的是葡萄糖 |
④ | 鉴别AlCl3 溶液和MgCl2溶液 | 氨水 | 产生白色沉淀然后消失的是AlCl3 溶液 |
A.①③ B.①② C.②④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
根据所学知识填写下列空白.
(1)用系统命名法命名: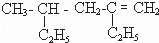 ;
;
(2)写出下列有机物的结构简式:2,6﹣二甲基﹣4﹣乙基辛烷: ;
(3)写出下列反应的化学方程式并分别指出其反应类型:
①将苯与浓硫酸和浓硝酸的混合液共热: ;反应类型为: ;
②1﹣丁烯与氯化氢反应: ;反应类型为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:2SO2(g)+O2(g)⇌2SO3(g)△H=﹣196.6kJ•mol﹣1,向密闭容器中加入2mol SO2(g)和1mol O2,一定条件下反应达到平衡,在t2和t4时刻分别只改变一个条件(温度或压强),反应过程中正反应速率如下图所示,下列说法正确的是( )注:t1~t2、t3~t4、t5之后各时间段表示达到平衡状态①、②、③.
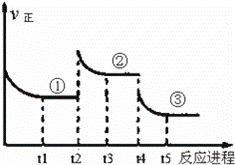
|
| A. | t2~t3时间段,平衡向逆反应方向移动 |
|
| B. | 平衡状态①和②,平衡常数K值相同 |
|
| C. | 平衡状态①和②,SO2转化率相同 |
|
| D. | t4时刻改变的条件是减小压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
H﹣H、Cl﹣Cl和H﹣Cl的键能分别为436、243和431kJ/mol.请用此数据估计由Cl2、H2反应生成1molHCl时的热效应()
A. 放热183 kJ B. 放热91.5 kJ C. 吸热183 kJ D. 吸热91.5 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
暗紫色化合物A可作为电极材料的新型超铁电磁,因具有绿色、高电压和高能量的特点,近年来引起了电化学界的高度重视.在常温和干燥的条件下,化合物A可以稳定的存在,但它在水溶液中不稳定,一段时间后转化为红褐色沉淀.为探究其成分,某学习兴趣小组的同学取化合物A粉末进行试验.经组成分析,该粉末仅含有O、K、Fe三种元素.
另取3.96g化合物A的粉末溶于水,滴加足量的稀硫酸,向反应后的溶液中加入含有0.08mol KOH的溶液,恰好完全反应.过滤,将洗涤后的沉淀充分灼烧,得到红棕色固体粉末1.60g;将所得滤液在一定条件下蒸发可得到一种纯净的不含结晶水的盐10.44g.
(1)3.96g化合物A中含有Fe元素的物质的量为0mol,含有钾元素的物质的量为mol.化合物A的化学式为;
(2)化合物A与H2O反应的离子方程式为:.
(3)为研究温度对化合物A水溶液稳定性的影响,请设计一个实验方案..
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com