
已知A、B、C、D、E都是含氮元素的化合物,有下列几个反应(未配平):
①A+O2→C ②C+H2O→A+B ③D+O2→A+H2O ④A+C+NaOH→E+H2O写出上述五种化合物的分子式:
A是 ,B是 ,C是 ,D是 ,E是
(2)某同学写出下面四个不同价态的氮的化合物相互转换的关系(未配平):
A.NO+HNO3→N2O3+H2O
B.NH3+NO→HNO2+H2O
C.N2O4+H2O→HNO3+HNO2
D.NH3+HNO2→N2+H2O
其中你认为一定不可能实现的是 (填字母编号).
考点:
氧化还原反应方程式的配平.
专题:
氧化还原反应专题.
分析:
(1)由于氮的化合物C能够和水反应生成两种物质A和B,②C+H2O→A+B,A又能氧化生成C①A+O2→C,可推知C为NO2 ,A为NO,B为HNO3,再根据③D+O2→A+H2O可推知D为NH3 ,根据④A+C+NaOH→E+H2O推知E为NaNO2 ;
(2)有元素化合价变化的反应为氧化还原反应,在氧化还原反应中元素的化合价由升高的就必然有降低的,并且化合价的升降相等,如果一个反应中只有元素化合价的升高没有降低或者只有化合价的降低没有升高,这个反应一定不能实现.
A.NO+HNO3→N2O3+H2O,N元素化合价有升有降,此反应可能实现;
B.NH3+NO→HNO2+H2O,N元素的价态只有升高没有降低,一定不可能实现;
C.N2O4+H2O→HNO3+HNO2,N元素化合价有升有降,此反应可能实现;
D.NH3+HNO2→N2+H2O,N元素化合价有升有降,此反应可能实现.
解答:
解:(1)由于氮的化合物C能够和水反应生成两种物质A和B,②C+H2O→A+B,A又能氧化生成C①A+O2→C,可推知C为NO2 ,A为NO,B为HNO3,再根据③D+O2→A+H2O可推知D为NH3 ,根据④A+C+NaOH→E+H2O推知E为NaNO2;
故答案为:NO;HNO3;NO2;NH3;NaNO2;
(2)有元素化合价变化的反应为氧化还原反应,在氧化还原反应中元素的化合价由升高的就必然有降低的,并且化合价的升降相等,如果一个反应中只有元素化合价的升高没有降低或者只有化合价的降低没有升高,这个反应一定不能实现.
A.NO+HNO3→N2O3+H2O,N元素化合价有升有降,此反应可能实现,故A不选;
B.NH3+NO→HNO2+H2O,N元素的价态只有升高没有降低,一定不可能实现,故可选;
C.N2O4+H2O→HNO3+HNO2,N元素化合价有升有降,此反应可能实现,故A不选;
D.NH3+HNO2→N2+H2O,N元素化合价有升有降,此反应可能实现,故A不选;
故答案为:B.
点评:
本题考查无机物的推断和氧化还原反应的判断,结合物质的转化关系解答该题,牢固掌握常见元素化合物的性质为解答该题的关键.题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
)某班学生分成甲,乙两小组分别探究硫,氮及其化合物的性质:
(一)甲组同学用图1装置来探究浓硫酸与木炭粉加热反应并验证反应所产生的各种产物.
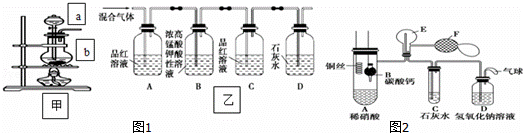
(1)装置甲中盛放浓硫酸的仪器a名称是 ,装置甲中仪器b中发生反应的化学方程式为
(2)实验中可观察到装置乙中,A瓶的溶液褪色,C瓶的溶液不褪色.
A瓶溶液的作用是 ,
D瓶溶液的现象是 .
(二)乙组同学用图2装置来证明铜与稀硝酸反应产生一氧化氮,B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球.(1)实验时,先将B装置下移,使碳酸钙与稀硝酸接触产生气体,当C处产生白色沉淀时,立刻将B装置上提,使之与稀硝酸分离.该组学生设计此步操作的目的是 .
(2)装置E中开始时出现浅红棕色气体,用F向E中鼓入空气后,可观察到烧瓶E内气体颜色加深,产生上述现象的原因是 .
(3)一段时间后,C中白色沉淀溶解,其原因是
(4)装置D的作用是
查看答案和解析>>
科目:高中化学 来源: 题型:
实验:用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.
(1)由上述实验现象所得出的有关过氧化钠跟水反应的结论是:
第一,有氧气生成,第二, .Na2O2跟水反应的化学方程式是 .
(2)某研究性学习小组拟用A图所示装置(气密性良好)进行实验,以证明上述结论.用以验证第一条结论的实验方法是: ;用以验证第二条结论的实验方法是: .
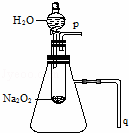
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,则下列叙述正确的是( )
|
| A. | 常温下,4.48L N2和O2的混合气体中所含原子数为0.4NA |
|
| B. | 常温下,1.0L1.0mol•L﹣1 NaAlO2溶液中含有的氧原子数为2NA |
|
| C. | 7.8g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA |
|
| D. | 0.1mol Fe参加氧化还原反应,转移的电子数目一定是0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
ClO2是一种广谱型的消毒剂,根据世界环保联盟的要求,ClO2将逐渐取代Cl2成为生产自来水的消毒剂.工业上ClO2常用NaClO3和Na2SO3溶液混合并加H2SO4酸化后反应制得,其中Na2SO3被氧化为Na2SO4.在以上反应中,NaClO3和Na2SO3的物质的量之比为( )
|
| A. | 1:1 | B. | 2:1 | C. | 1:2 | D. | 2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应NaClO+2HCl=NaCl+H2O+Cl2↑,被氧化的氯原子与被还原的氯原子之比是( )
|
| A. | 1:1 | B. | 1:2 | C. | 2:1 | D. | 3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数,下列说法正确的是()
A. 1 mol氯气参加氧化还原反应,转移的电子数一定为2NA
B. 常温常压下,由6 g NO2和40 g N2O4组成的混合气体中原子总数为3NA
C. 0.1 mol•L﹣1 NaF溶液中,HF和F﹣总和为0.1NA个
D. 12.5 mL 16 mol•L﹣1浓硫酸与足量铜反应,生成SO2的分子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上用改进汽油组成的办法来改善汽油的燃烧性能,例如:加入CH3OC(CH3)3来生产无铅汽油.CH3OC(CH3)3分子中必存在的原子间连接形式是( )
A. 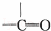 B.
B. 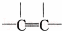 C.
C. 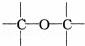 D.
D. 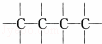
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com