
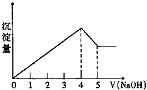
 有一镁、铝合金,用适量稀硫酸完全溶解,再加入氢氧化钠溶液,析出沉淀的质量随氢氧化钠的体积关系如图所示,原合金中镁、铝质量比为( ) (Mg、Al的相对原子质量分别为24、27)
有一镁、铝合金,用适量稀硫酸完全溶解,再加入氢氧化钠溶液,析出沉淀的质量随氢氧化钠的体积关系如图所示,原合金中镁、铝质量比为( ) (Mg、Al的相对原子质量分别为24、27)| A、4:3 | B、4:9 |
| C、8:9 | D、20:27 |


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:
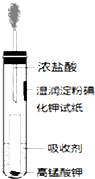 氯气是氯碱工业的主要产品之一,是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:Cl2+H2O?HCl+HClO K=4.5×10-4
氯气是氯碱工业的主要产品之一,是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:Cl2+H2O?HCl+HClO K=4.5×10-4查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe(NO3)3、NaOH、CuSO4、KCl |
| B、KCl、AgNO3、HCl、HNO3 |
| C、CuSO4、NaCl、KNO3、BaCl2 |
| D、BaCl2、Na2SO4、Na2CO3、HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaOH |
| B、FeSO4 |
| C、BaCl2 |
| D、NaClO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| NaOH的质量分数 | 阳极析出物质的质量/g | 阴极析出物质的质量/g | |
| A | 0.062(6.2%) | 19 | 152 |
| B | 0.062(6.2%) | 152 | 19 |
| C | 0.042(4.2%) | 1.2 | 9.4 |
| D | 0.042(4.2%) | 9.4 | 1.2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用量筒量取所需的浓硫酸时仰视读数 |
| B、定容后摇匀,发现液面最低点低于刻度线,再补加几滴蒸馏水至刻度线 |
| C、定容时,俯视刻度线 |
| D、用量筒量取浓硫酸倒入烧杯,再用蒸馏水洗量筒2~3次,洗液倒入烧杯中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述正确的是:
如图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述正确的是:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com