
①CO2 ②HCl ③H2O(g) ④O2
A.①②③ B.②③④ C.②③ D.①④
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案科目:高中化学 来源: 题型:013
已知浓盐酸和次氯酸钙发生如下反应:
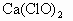 +4HCl(浓)=
+4HCl(浓)=若用贮存很久的漂白粉与浓盐酸反应制氯气,则可能含有的杂质气体是
[ ]
①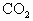 ②CO ③
②CO ③![]() ④HCl
④HCl
查看答案和解析>>
科目:高中化学 来源:最新名师点评测试卷(高一) 题型:013
已知浓盐酸和次氯酸钙发生如下反应:
 +4HCl(浓)=
+4HCl(浓)=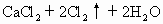
若用贮存很久的漂白粉与浓盐酸反应制氯气,则可能含有的杂质气体是
[ ]
①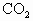 ②CO③
②CO③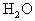 ④HCl
④HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
A.HCl B.H2O(g) C.O2 D.CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
(8分)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
(1)用方程式表示工业上用石灰石、氯气为原料生产漂白粉的原理_________________
_______________________________________________________,漂白粉的有效成分是(填化学式)
(2)漂白粉可用于饮用水或环境消毒,它溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,写出相应的化学方程式:___________________
(3)浓盐酸和次氯酸钙能发生下列反应:Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O,该反应中转移的电子数为___________
A.①②③ B.②③④ C.②③ D.①④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com