
用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴、阳离子交换膜组合循环再生机理如下图所示,则下列有关说法中不正确的是
A.X为直流电源的负极,Y为直流电源的正极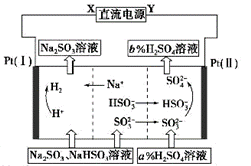
B.阳极区pH增大
C.图中的b>a
D.该过程中的产品主要为H2SO4和H2
科目:高中化学 来源: 题型:
铜是人类认识并应用最早的金属之一,我国是最早使用铜器的国家之一。铁与人类生活密切相关,几乎无处不在,是地壳中含量仅次于铝的金属。某研究性学习小组为了证明铁的金属活动性比铜强,设计了如下实验方案:
(1)将铁片置于硫酸铜溶液中有铜析出
(2)铁、铜和氯气反应分别生成FeCl3和CuCl2
(3)足量的铁粉和铜粉与浓硫酸在加热条件下反应分别生成FeSO4和CuSO4
(4)将铜片置于FeCl3溶液中铜片逐渐溶解
(5)把铁片和铜片置于盛有稀硫酸的烧杯中,并用导线连接,铁片上无气泡产生,而铜片上有气泡产生
(6)把铁片和铜片置于盛有浓硝酸的烧杯中,并用导线连接,铁片上有气泡产生,而铜片上无气泡产生
以上实验方案设计合理的有( )
A.两种 B.三种
C.四种 D.五种
查看答案和解析>>
科目:高中化学 来源: 题型:
用两根铂丝作电极插入KOH溶液中,再分别向两极通入甲烷气体和氧气,可形成燃料电池,该电池放电时的总反应为:CH4+2KOH+2O2=K2CO3+3H2O,下列说法错误的是
A. 通甲烷的一极为负极,通氧气的一极为正极
B. 放电时通入氧气的一极附近溶液的pH升高
C. 放电一段时间后,KOH的物质的量不发生变化
D. 通入甲烷一极的电极反应式是:CH4+10OH --8e-=CO32-+7H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
有关右图的说法正确的是
A.构成原电池时溶液中SO42- 移向Cu极
B.构成原电池时Cu极反应为: Cu﹣2e-=Cu2+
C.要使Fe极不被腐蚀,Cu片换Zn片或a接直流电源负极
D.形成电解池,Cu电极不可能溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
2013年7月23日,央视记者分别在北京崇文门附近的麦当劳、肯德基以及真功夫3家大型快餐店取回可食用冰块进行抽样检测。检测结果显示:
3家快餐店食用冰块菌落总数严重超标。下列说法正确的是
A.肉毒杆菌有毒,可在其中加入硫酸铜使其变性后食用
B.肉毒杆菌在体内水解生成的氨基酸不能成为人体重要的营养物质
C.大肠杆菌分子中不一定含羧基和氨基
D.出血性大肠杆菌和油脂均为能水解的高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【化学——选修2:化学与技术】(15分)
化学是人类进步的关键,化学为人类的生产、生活提供了物质保证。
(1)电镀时,用镀层金属作阳极的作用是 .
为了使镀层厚度均匀、光滑致密、与镀件的附着力强,除控制溶液中离子浓度外,
通常还可以采取的措施有 。
(2)卤水中蕴含着丰富的镁资源,经转化后可获得MgCl2粗产品。从卤水中提取镁的
步骤为:
a.将海边大量存在的贝壳煅烧成石灰,并将石灰制成石灰乳;
b.将石灰乳加入到海水沉淀池中经过滤得到Mg(OH)2沉淀;
c.在Mg(OH)2沉淀中加入盐酸得到MgCl2溶液,再经蒸发结晶得到MgCl2·6H2O;
d.将MgCl2·6H2O在一定条件下加热得到无水MgCl2;
e.电解熔融的氯化镁可得到Mg。
①步骤d中的“一定条件”指的是 ,目的是 。
上述提取镁的流程中,为了降低成本.减少污染,可以采取很多措施,请写出其中一点
②有同学认为:步骤b后可加热Mg(OH)2得到MgO,再电解熔融的MgO制金属镁,这样可简化实验步骤,你同意该同学的想法吗?为什么?
(3)铀是核反应最重要的燃料,已经研制成功一种螫合型离子交换树脂,它专门吸附海水中 的U4+,而不吸附其他元素。其反应原理为 (树脂用HR代替),发生离子交换后的离子交换膜用酸处理还可再生并得到含铀的溶液,其反应原理为: 。
(4)阿司匹林(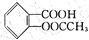 )在潮湿空气中可分解成水杨酸和醋酸而略带酸臭味,故密封保存,用化学方程式表示阿司匹林必须贮藏于密闭、干燥处的原因:
)在潮湿空气中可分解成水杨酸和醋酸而略带酸臭味,故密封保存,用化学方程式表示阿司匹林必须贮藏于密闭、干燥处的原因:
,此反应的类型属于 。
查看答案和解析>>
科目:高中化学 来源: 题型:
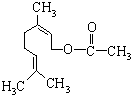
乙酸橙花酯是一种食用香料,结构如图所示。下列关于该有机物的说法有如下几种:
①该有机物有一种同分异构体属于酚类;
②该有机物属于酯类;
③该有机物不能发生银镜反应;
④该有机物的分子式为C11H18O2;
⑤1mol该有机物最多能与1mol NaOH反应。其中正确的是
A.①③④ B.②③⑤ C.①④⑤ D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
OH-不能和________________________________________________________大量共存(填具体离子,下同)。
查看答案和解析>>
科目:高中化学 来源: 题型:
某pH=1的工业废液,只可能含有以下离子中的若干种:H+、Mg2+、Ba2+、Cl-、CO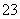 、SO
、SO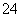 ,现取两份100 mL溶液进行如下实验:
,现取两份100 mL溶液进行如下实验:
第一份加入足量AgNO3溶液,得干燥沉淀3.50 g。
第二份加入足量BaCl2溶液后,得干燥沉淀2.33 g,经足量盐酸洗涤、干燥后,沉淀质量不变。
根据上述实验,以下推测正确的是 ( )
①一定存在Mg2+ ②可能存在CO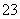 ③一定存在Cl- ④可能存在Ba2+ ⑤可能存在Mg2+
③一定存在Cl- ④可能存在Ba2+ ⑤可能存在Mg2+
A.①③ B.②③
C.③⑤ D.④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com