
分析 萤石和浓硫酸反应方程式为CaF2+H2SO4=CaSO4+2HF,根据氟化钙和HF之间的关系式计算生成HF溶液质量;根据氟化钙和浓硫酸的关系式计算消耗浓硫酸质量.
解答 解:设生成40%HF溶液的质量是x,消耗96%的浓硫酸y,
CaF2+H2SO4=CaSO4+2HF
78g 98g 40g
8000kg×80%×85% 96%y 40%x
78g:98g=8000kg×80%×85%:96%y,
y=$\frac{8000kg×80%×85%×98g}{78g×96%}$=7120kg,
78g:40g=8000kg×80%×85%:40%x
x=$\frac{8000kg×80%×85%×40g}{78g×40%}$=6564kg,
答:能制得40%(质量分数)HF溶液6564千克;同时要消耗96%(质量分数)H2SO47120千克.
点评 本题考查化学方程式有关计算,为高频考点,明确各个物理量关系是解本题关键,计算量较大,但题目难度不大.


 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源: 题型:选择题
| A. | 三处 | B. | 四处 | C. | 五处 | D. | 六处 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 和一个-Cl,它的可能结构分别是(填写结构简式):CH3CH2CH2CHClCH3、CH3CH2CHClCH2CH3、CH3CH(CH3)CH2CH2Cl、CH2ClCH(CH3)CH2CH3.
和一个-Cl,它的可能结构分别是(填写结构简式):CH3CH2CH2CHClCH3、CH3CH2CHClCH2CH3、CH3CH(CH3)CH2CH2Cl、CH2ClCH(CH3)CH2CH3.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
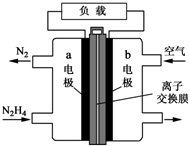 氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
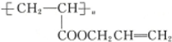 ,则醇A的结构简式为 ( )
,则醇A的结构简式为 ( )| A. | CH3CH2CH2OH | B. | CH2═CHCH2OH | C. | 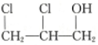 | D. | 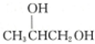 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com