


科目:高中化学 来源: 题型:
| A、减小压强 |
| B、缩小体积 |
| C、降低温度 |
| D、增大H2的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
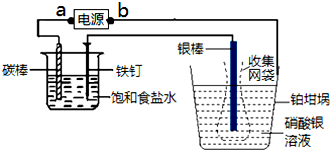
| A、a为电源的负极,铂坩埚为阳极 |
| B、称量电解前后铂坩埚的质量变化,得金属银的沉积量为108.0 mg,则电解过程中通过电解池的电量为96500C |
| C、实验中,为了避免银溶解过程中可能产生的金属颗粒掉进铂坩埚而导致测量误差,常在银电极附近增加一个收集网袋.若没有收集网袋,测量结果会偏高 |
| D、铁钉和碳棒上都有气泡产生,若加入酚酞试剂,先在碳棒附近溶液变红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
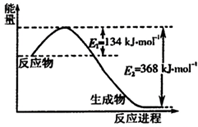 氮是一种地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义.
氮是一种地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝片与稀H2SO4反应 |
| B、Ba(OH)2?8H2O与NH4Cl的反应 |
| C、灼热的炭与CO2反应 |
| D、甲烷在O2中的燃烧反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、CuO+CO
| ||||
| B、2KClO3+I2═2KIO3+Cl2 | ||||
| C、O3+Na2SO3═Na2SO4+O2 | ||||
| D、2FeCl3+2HI═I2+2FeCl2+2HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com