
下面有关金属的叙述正确的是( )
A.金属受外力作用时常常发生变形而不易折断,是由于金属离子之间有较强的作用
B.通常情况下,金属中的自由电子会发生定向移动,而形成电流
C.金属是借助金属离子的运动,把能量从温度高的部分传到温度低的部分
D.金属的导电性随温度的升高而降低
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
据报道,科学家成功制得了CO2的原子晶体(以下用M表示)。下列关于M的推断正确的是( )
A.M具有很高的熔、沸点
B.M容易气化,可用作致冷材料
C.M和干冰互为同素异形体
D.M是由C原子和O原子按1∶2的比例所组成的平面网状的晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
碱金属卤化物是典型的离子晶体,它们的晶格能与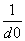 成正比(d0是晶体中最邻近的带有异性电荷离子的核间距)。下面说法错误的是( )
成正比(d0是晶体中最邻近的带有异性电荷离子的核间距)。下面说法错误的是( )
| 晶格能/kJ·mol-1 | 离子半径/pm | |
| ① | LiF LiCl LiBr LiI 1 031 845 807 752 | Li+ Na+ K+ 60 95 133 |
| ② | NaF NaCl NaBr NaI 915777 740 693 | F- Cl- Br- I- 136 181 195 216 |
| ③ | KF KCl KBr KI 812 708 676 641 |
A.晶格能的大小与离子半径成正比
B.阳离子相同、阴离子不同的离子晶体,阴离子半径越大,晶格能越小
C.阳离子不同、阴离子相同的离子晶体,阳离子半径越小,晶格能越大
D.金属卤化物晶体中,晶格能越小,还原性越强
查看答案和解析>>
科目:高中化学 来源: 题型:
石墨晶体具有一些独特的性质,质地较柔软但熔点很高,还具有导电性,这主要是因为石墨晶体具有一种独特的结构,石墨晶体是( )
A.原子晶体 B.金属晶体
C.分子晶体 D.混合键型晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般地为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如[Co(H2O)6]2+显粉红色。据此判断,[Mn(H2O)6]2+_______颜色(填“无”或“有”)。
(2)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。
①COCl2分子的结构式为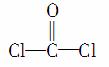 ,对其所存在的共价键,下列说法正确的是( )
,对其所存在的共价键,下列说法正确的是( )
A.4个σ键
B.2个σ键、2个π键
C.2个σ键、1个π键
D.3个σ键,1个π键
②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5===Fe(s)+5CO↑,反应过程中,断裂的化学键只有____________。形成的化学键是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.分子晶体中的每个分子内一定含有共价键
B.原子晶体中的相邻原子间只存在非极性共价键
C.离子晶体中可能含有共价键
D.金属晶体的熔点和沸点都很高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com