
| A. | 4:13 | B. | 1:13 | C. | 1:3 | D. | 13:4 |
分析 Na+的物质的量为0.01mol,Fe3+的物质的量为0.04mol,由电荷守恒可知,Cl-的物质的量为0.01+0.04×3=0.13mol,在此溶液中加入0.03mol氢氧化钠,则最后溶液中的Na+为0.04mol,而Cl-不变,以此来解答.
解答 解:Na+的物质的量为0.01mol,Fe3+的物质的量为0.04mol,由电荷守恒可知,Cl-的物质的量为0.01+0.04×3=0.13mol,在此溶液中加入0.03mol氢氧化钠,溶液中的Na+为0.04mol,而Cl-不变,则最后溶液中的Na+与Cl-的数目之比为0.04mol:0.13mol=4:13,
故选A.
点评 本题考查物质的量的计算,为高频考点,把握电荷守恒及离子的变化为解答的关键,侧重分析与计算能力的考查,注意电荷守恒的应用,题目难度不大.


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:选择题
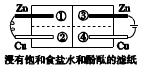
| A. | 两处的锌片均发生氧化反应 | |
| B. | 左侧铜片上的电极反应为2H2O+O2+4e-═4OH- | |
| C. | 阳离子移动方向分别由②→①、③→④ | |
| D. | 最先观察到红色的区域是④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2与酸性KMnO4溶液的反应:5SO2+2MnO4-+2H2O═5SO42-+2Mn2++4H+ | |
| B. | 稀硫酸和氢氧化钡溶液反应:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| C. | 硝酸银溶液中滴加过量氨水:Ag++NH3•H2O═AgOH↓+NH4+ | |
| D. | 石灰水与过量碳酸氢钠溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3种溶液pH的大小顺序是 ③>②>① | |
| B. | 若将3种溶液稀释相同倍数,pH变化最大的是① | |
| C. | 若分别加入25mL 0.1mol•L-1盐酸后,pH最小的是② | |
| D. | 若升高温度,则③的pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Al3+、Cl- | B. | K+、H+、SO42- | C. | Na+、HCO3-、NO3- | D. | K+、Na+、AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用丁达尔现象区分溶液与胶体 | |
| B. | 用蒸馏的方法除去自来水中含有的Cl- | |
| C. | 用萃取的方法从某些植物中提取香料或中药成份 | |
| D. | 金属钠长期暴露在空气中的最终产物是NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c=$\frac{Vρ}{17V+22400}$ | B. | ω=$\frac{17c}{100ρ}$ | ||
| C. | ω=$\frac{17V}{17V+22400}$ | D. | ρ=$\frac{17V+22400}{22.4+22.4V}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg和Al都可以用电解法冶炼得到 | |
| B. | Na2O2、Na2O组成元素相同,与CO2反应产物也相同 | |
| C. | 用过量的KSCN溶液除去FeCl2溶液中的少量FeCl3 | |
| D. | Na和Fe在一定条件下与水反应都生成H2和对应的碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1:1 | B. | 4:4:5 | C. | 5:5:4 | D. | 无法确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com