
 ,
, ;
;

科目:高中化学 来源: 题型:
| A、C原子的四个杂化轨道的能量一样 |
| B、C原子的sp3杂化轨道之间夹角一样 |
| C、C原子有1个sp3杂化轨道由孤电子对占据 |
| D、C原子的4个价电子分别占据4个sp3杂化轨道 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHCO3═Na++H++CO32- |
| B、Al2(SO4)3═2Al3++3SO42- |
| C、NaHS?Na++HS- |
| D、Ca(OH)2═Ca2++(OH)22- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、聚丙烯的链节:-CH2-CH2-CH2- | ||
B、NH4Cl的电子式: | ||
C、F-结构示意图: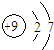 | ||
D、中子数为20的氯原子:
|
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 将一个装有饱和石灰水的试管放入盛有25℃饱和石灰水的广口瓶中,如图所示.
将一个装有饱和石灰水的试管放入盛有25℃饱和石灰水的广口瓶中,如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com