
【题目】下列物质进行一氯取代后,生成的产物只有2种的是
A.(CH3)2CHCH(CH3)2
B.(CH3)3CCH2CH3
C.(CH3CH2)2CHCH3
D.(CH3)4C
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】—定温度下,难溶电解质的饱和溶液中存在沉淀溶解平衡,己知:
物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
KSP(25℃) | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
25℃时,对于CuSO4、FeSO4、Fe2(SO4)3各0.5mol的1L混合溶液,根据上表数据断,下列说法不正确的是( )
A. 向混合溶液中加入适量氨水,并调节pH在3~4后过滤,可获得纯净的CuSO4溶液
B. 向混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀
C. 该溶液中c(SO42-):[c(Cu2+)+ c(Fe2+)+c(Fe3+)]>5:4
D. 在pH=5的溶液中.Fe3+不能大量存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的工业废水中含有大量的“FeSO4”、较多的Cu2+和少量的Na+。为了减少污染变废为宝,工厂计划从该废水中回收硫酸亚铁和铜。根据流程图,完成回收硫酸亚铁和铜的简单实验方案。回答下列问题:

(1)加入原料①为____________;操作②为___________;
(2)固体A为____________;
(3)写出有关反应的化学方程式__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.1mol·L-1CH3COOH溶液中存在如下电离平衡:CH3COOH![]() CH3COO-+H+对于该平衡,下列叙述正确的是 ( )
CH3COO-+H+对于该平衡,下列叙述正确的是 ( )
A. 加入水时,平衡向逆反应方向移动
B. 加入少量NaOH固体,平衡向正反应方向移动
C. 加入少量0.1mol·L-1HCl溶液,溶液中c(H+)减小
D. 加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cl2与CH4在光照条件下,按照体积比1:1反应,则生成的产物为
A.CH3ClB.CH2Cl2C.HClD.CH3Cl、CH2Cl2、CHCl3、CCl4、HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常状况下,下列物质中①硫酸钡 ②醋酸 ③氯化氢 ④三氧化硫 ⑤氯气 ⑥碳酸钠 ⑦铜 ⑧硫酸溶液 ⑨氢氧化钾 ⑩乙醇(下列各空填序号)
(1)属于强电解质的是:________________。
(2)属于弱电解质的是:________________。
(3)能导电的是:________________。
(4)属于非电解质的是:________________。
(5)碳酸钠溶液显碱性的原因________(用离子方程式表达)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸是重要的化工材料,二氧化硫生成三氧化硫是工业制硫酸的重要反应之一。
(1)将0.050 mol SO2和0.030 mol O2放入容积为1 L的密闭容器中,反应2SO2(g)+O2(g)![]() 2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040 mol/L。
2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040 mol/L。
①从平衡角度分析采用过量O2的目的是________________________;
②计算该条件下反应的平衡常数K=________________________。
③已知:K(300℃)>K(350℃),该反应是________热反应。若反应温度升高,SO2的转化率________ (填“增大”、“减小”或“不变”)。
(2)某温度下,SO2的平衡转化率(![]() )与体系总压强(P)的关系如图1所示。平衡状态由A变到B时,平衡常数K(A)_____K(B)(填“>”、“<”或“=”,下同)。
)与体系总压强(P)的关系如图1所示。平衡状态由A变到B时,平衡常数K(A)_____K(B)(填“>”、“<”或“=”,下同)。
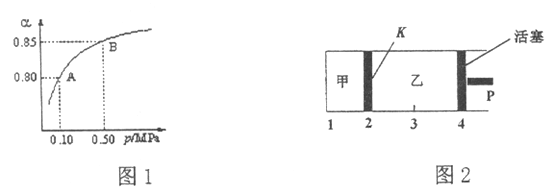
(3)如图2所示,保持温度不变,将2 mol SO2和1 mol O2加入甲容器中,将4 mol SO3加入乙容器中,隔板K不能移动。此时控制活塞P,使乙的容积为甲的2倍。
①若移动活塞P,使乙的容积和甲相等,达到新平衡时,SO3的体积分数甲______乙。
②若保持乙中压强不变,向甲、乙容器中通入等质量的氦气,达到新平衡时,SO3的体积分数甲_______乙。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是以有机物A合成聚酯类高分子化合物F的路线:

已知:
回答下列问题:
(1)A生成B的反应类型为_____,C中的官能团名称为________。
(2)D与NaOH水溶液反应的化学方程式为________。
(3)①E生成F的化学方程式为________。
②若F的平均相对分子质量为20000,则其平均聚合度为________。(填字母)
A.54 B.108 C.119 D.133
(4)E在一定条件下还可以合成含有六元环状结构的G。G的结构简式为________。
(5)满足下列条件的C的同分异构体有_____种。(不考虑立体异构)
①含有1个六元碳环且环上相邻4个碳原子上各连有一个取代基
②1mol该物质与斐林试剂反应产生2mol砖红色沉淀
(6)写出用![]() 为原料制各化合物
为原料制各化合物 的合成路线______。(其他试剂任选)
的合成路线______。(其他试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探索工业中铝、铁、铜的合金废料的再利用,某同学设计了如下回收方案:
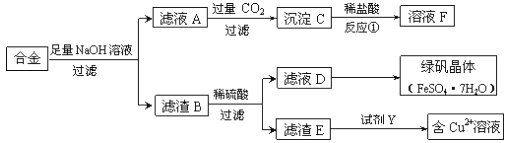
(1)操作①的名称是______________,滤渣B含有_______________(填化学式)。
(2)反应①的离子方程式是_________________________________。
(3)若要从滤液D中得到绿矾晶体,必须进行的实验操作是______________、冷却结晶、过滤、自然干燥,这一系列操作中没有用到的仪器有________(填序号)。
A.漏斗 B.坩埚 C.烧杯 D.玻璃棒
(4)试剂Y应该是一种________(填“氧化剂”或“还原剂”),它不可能是____(填序号)。
A.过氧化氢 B.氢气 C.氧气 D.铁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com