


科目:高中化学 来源: 题型:
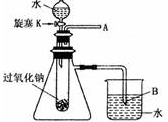 用脱脂棉包住约0.2g过氧化钠固体粉末,置于石棉网上,然后向包有过氧化钠的位置滴加几滴水,结果脱脂棉剧烈燃烧起来.
用脱脂棉包住约0.2g过氧化钠固体粉末,置于石棉网上,然后向包有过氧化钠的位置滴加几滴水,结果脱脂棉剧烈燃烧起来.查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
A、
| ||
B、
| ||
| C、7 | ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑤ | B、①②⑤ |
| C、②④⑤ | D、②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe3+,NH4+,SCN-,Cl- |
| B、Na+,H+,NO3-,SO42- |
| C、Fe2+,H+,Na+,NO3- |
| D、Fe2+,NH4+,Cl-,OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
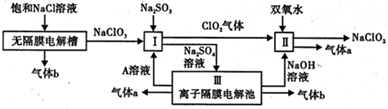
查看答案和解析>>
科目:高中化学 来源: 题型:
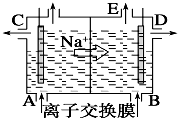
| A、从E口逸出的气体是H2 |
| B、从B中加入含少量NaOH的水溶液以增强导电性 |
| C、标准状况下每生成22.4LCl2,便产生2molNaOH |
| D、完全电解后加适量盐酸可以恢复到电解前的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、平衡向右移动 |
| B、B的转化率提高 |
| C、x+y>z |
| D、C的体积分数增加 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、物质在反应中失去电子,该物质是氧化剂 |
| B、任何一个置换反应一定属于氧化还原反应 |
| C、有单质生成的化学反应一定是氧化还原反应 |
| D、在反应中一种物质被氧化,另一种物质一定被还原 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com