
【题目】下列说法正确的是
A.75%的酒精可使蛋白质变性,常用于杀菌消毒
B.氨基酸为高分子化合物,分子中含有-COOH和-NH2
C.往淀粉水解液中加入过量NaOH溶液,再加入碘水,未变蓝色,则说明淀粉已完全水解
D.油脂在碱性条件下水解生成高级脂肪酸和甘油
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】铅蓄电池是常见的二次电池,电池总反应为:Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O下列说法正确的是
2PbSO4+2H2O下列说法正确的是
A. 放电时PbO2发生氧化反应
B. 充电时电解质溶液的质量减少
C. 放电时的负极反应式为Pb+SO42--2e-= PbSO4
D. 充电时的阴极反应式为PbSO4+2H2O-2e-= PbO2+SO42-+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烷烃的结构简式为

(1)用系统命名法命名该烃:______________________________________。
(2)若该烷烃是由烯烃加氢得到的,则原烯烃的结构有___________种。(不包括立体异构,下同)
(3)若该烷烃是由炔烃加氢得到的,则原炔烃的结构有____________ 种。
(4)该烷烃在光照条件下与氯气反应,生成的一氯代烷最多有_______ 种。
(5)写出由甲苯制取TNT的反应方程式______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中用KClO3在MnO2催化下受热分解制取氧气;从反应后的KCl和MnO2的混合物中分离、回收这两种物质。
(1)写出KClO3在MnO2催化下受热分解制取氧气的化学方程式:____________________;
(2)从KCl和MnO2的混合物中分离、回收这两种物质的实验方案如下:
![]()
步骤②的名称为______________,MnO2固体的洗涤方法______________________;
(3)步骤③的名称为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素R、X、Y、Z 在周期表中的相对位置如图所示。已知: Y的最高价氧化物对应的水化物既能与强碱反应,又能与强酸反应。下列说法不正确的是
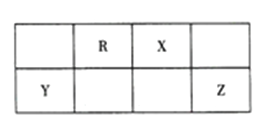
A. 简单气态氢化物的热稳定性: R<X
B. Y、Z的简单离子在同一溶液中能大量共存
C. 工业上,采用电解法冶炼单质Y
D. RZ2是含极性键的共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.有机物的结构可用“键线式”简化表示.CH3-CH=CH-CH3可简写为![]() .有机物X的键线式为:
.有机物X的键线式为:
(1)有机物Y是X的同分异构体,且属于芳香烃,写出Y的结构简式_______________;
(2)Y在一定条件下发生聚合反应,写出其反应的化学方程式_______________________;
(3)二甲苯苯环上的一溴代物有6种同分异构体,这些一溴代物与生成它们的对应二甲苯的熔点分别为:
一溴代二甲苯 | 234℃ | 206℃ | 213.8℃ | 204℃ | 214.5℃ | 205℃ |
对应二甲苯 | 13℃ | -54℃ | -27℃ | -54℃ | -27℃ | -54℃ |
由以上数据推断:
熔点为234℃的一溴代二甲苯的结构简式为____________;熔点为-27℃的二甲苯的名称为____________;
II.治疗甲型H1N1流感的常见药物有奥司他韦、扎那米韦、金刚乙胺及金刚烷胺以及预防药物如中药材金银花、大青叶等。其中金刚烷胺可按下列路线合成:

已知狄尔斯阿德耳反应(也称双烯合成反应)如下所示:

试回答下列问题:
(1)B的结构式为________________(填键线式)。
(2)上述物质中,属于同分异构体的是________(填字母)。
(3)上述反应中,属于加成反应的是________(填数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛是一种现代工业应用广泛的优良金属,使用量可能会超过金属铁。工业上冶炼金属钛的方法有多种,下列反应原理是比较常见的冶炼钛的一种方法:
①TiO2+2Cl2 +2C![]() TiCl4+2CO;②TiCl4+2Mg
TiCl4+2CO;②TiCl4+2Mg ![]() Ti+2MgCl2。
Ti+2MgCl2。
请回答下列问题:
(1)与钛同周期元素中未成对电子数最多的基态原子的电子排布式为_________________。
(2)反应①中涉及的非金属元素电负性由大到小的顺序为_________(用元素符号表示);与CO互为等电子体的离子为__________(填化学式,写一种即可)。
(3)①TiCl4在常温下是无色液体,分子中4 个氯原子不在一个平面上,TiCl4空间构型为____,该物质能否溶解在苯溶剂中__________(填“能”或“否”) 。
②三氯化钛与酒石酸(![]() )反应,制得新的固态配合物酒石酸羟基钛(III)[Ti(OH)(C4H4O6)·1.5H2O),在酒石酸中,羧基氧原子的轨道杂化类型分别是_______,σ键和π键的数目比为__________,Ti3+能形成配合物的原因为____________。1个酒石酸分子中手性碳原子数有_____________个。
)反应,制得新的固态配合物酒石酸羟基钛(III)[Ti(OH)(C4H4O6)·1.5H2O),在酒石酸中,羧基氧原子的轨道杂化类型分别是_______,σ键和π键的数目比为__________,Ti3+能形成配合物的原因为____________。1个酒石酸分子中手性碳原子数有_____________个。
(4)钛酸钡晶体的结构示意图如图所示,若晶胞参数为a pm,则钛酸钡晶体的密度=_____g/cm3(阿伏加德罗常数用NA表示)。
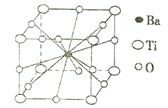
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是

A. 若A为H2O2,B为MnO2,C中盛有Na2S溶液, C中溶液变浑浊
B. 若A为浓盐酸,B为MnO2,C中盛有KI淀粉溶液,C中溶液变蓝色
C. 若A为浓氨水,B为生石灰,C中盛有AlCl 3溶液, C中先产生白色沉淀后沉淀又溶解
D. 若A为浓H2SO4 ,B为CaCO3,C中盛有Na2SiO3 溶液,C中溶液出现白色沉淀,证明非金属性S>C>Si
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com