
分析 根据题意可知4.66g固体是硫酸钡的质量,计算出其中的钡元素的质量,3.20g固体是Fe2O3的质量,计算出其中的铁元素的质量,混合氧化物中氧元素的质量=12.52g-钡元素的质量×2-铁元素的质量×2,通过n=$\frac{m}{M}$计算Ba、Fe、O三种元素的物质的量,根据物质的量的比值确定分子式.
解答 解:混合氧化物加入硫酸钾溶液得到白色沉淀,硫酸盐只有硫酸钡不溶,所以4.66g固体是硫酸钡的质量,则硫酸钡中钡元素的质量:4.66g×$\frac{137}{233}$×100%=2.74g,
混合氧化物中加入氢氧化钠得到红褐色沉淀,红褐色沉淀只有氢氧化铁,所以3.20g是Fe2O3的质量,则Fe2O3中铁元素的质量:3.20g×$\frac{112}{160}$×100%=2.24g,
所以氧元素质量:12.52g-2.74g×2-2.24g×2=2.56g,
n(Ba)=$\frac{2.74g×2}{137g/mol}$=0.04mol,n(Fe)=$\frac{2.24g×2}{56g/mol}$=0.08mol,n(O)=$\frac{2.56g}{16g/mol}$=0.16mol,
则分子式中N(Ba):N(Fe):n(O)=0.04mol:0.08mol:0.16mol=1:2:4,因此分子式为BaFe2O4,以氧化物的形式表示为BaO•Fe2O3,
故答案为:BaO•Fe2O3.
点评 本题考查复杂化学式的确定,侧重于元素化合物的性质的应用,解答本题的关键是要知道4.66g固体是硫酸钡的质量,3.20g固体是氢氧化铁的质量,题目难度中等.


科目:高中化学 来源: 题型:解答题
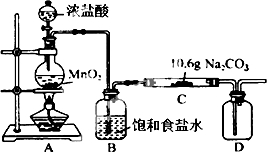 某化学活动小组设计如图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl2与Na2CO3反应得到的固体物质.
某化学活动小组设计如图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl2与Na2CO3反应得到的固体物质.| 步骤 | 预期现象和结论 |
| 步骤1:取C中少量样品于试管中,滴加足量蒸馏水 至溶解,然后将所得溶液分别置于A、B试管中 | 固体物质全部完全溶解 |
| 步骤:向A试管中滴加适量BaCl溶液 | a. 如果 b. 如果 |
| 步骤: | 有白色沉淀生成,C的部分有NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 生成氯气的相对分子质量为71 | B. | 生成1 mol氯化钾转移5 NA个电子 | ||
| C. | 生成氯化钾的摩尔质量为76 g/mol | D. | 1molH37Cl参加反应转移NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
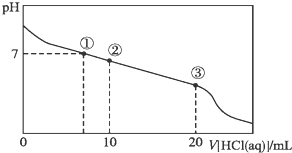
| A. | 点①所示溶液中,溶质为未反应完的CH3COONa、生成的CH3COOH和NaCl,微粒之间的关系为:c(CH3COOH)>c(Cl-)>c(OH-)=c(H+) | |
| B. | 点②所示溶液中,醋酸钠有一半与盐酸反应,微粒之间的关系为:c(Na+)>c(Cl-)>c(CH3COO-)>c(CH3COOH) | |
| C. | 点③所示溶液中,醋酸钠与盐酸恰好完全反应,微粒之间的关系为:c(Na+)>c(CH3COOH)>c(H+)>c(CH3COO-) | |
| D. | 整个过程中有可能出现:c(H+)+c(Na+)=c(CH3COOH)+c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
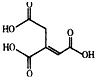
| A. | 化学式为C6H6O6 | |
| B. | 乌头酸能发生水解反应和加成反应 | |
| C. | 乌头酸能使酸性高锰酸钾溶液褪色 | |
| D. | 含1mol乌头酸的溶液最多可消耗3molNaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
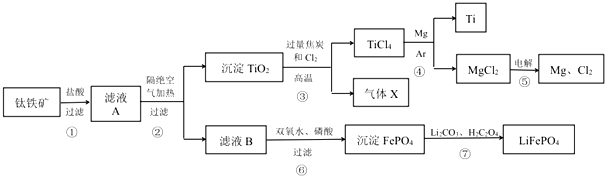
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 减压 | B. | 加压 | C. | 适当降温 | D. | 升高温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将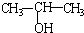 与NaOH的醇溶液共热制备CH3-CH=CH2 与NaOH的醇溶液共热制备CH3-CH=CH2 | |
| B. | 乙酰水杨酸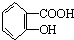 与适量NaOH溶液反应制备 与适量NaOH溶液反应制备 | |
| C. | 向CH3CH2Br中滴入AgNO3溶液以检验溴元素 | |
| D. | 苯酚在溴化铁催化作用下与液溴反应生成溴苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com