
【题目】某温度下,在容积为1L的密闭容器中充入![]() 和
和![]() 发生
发生![]() 测得
测得![]() 的物质的量随时间的变化如图所示,(已知,此温度下,该反应的平衡常数
的物质的量随时间的变化如图所示,(已知,此温度下,该反应的平衡常数![]() )下列说法正确的是 ( )
)下列说法正确的是 ( )
A. ![]()
B. 点b所对应的状态为化学平衡状态
C. ![]() 的生成速率,点a低于点b
的生成速率,点a低于点b
D. 欲增大平衡状态时![]() ,可保持其他条件不变,升高温度
,可保持其他条件不变,升高温度
【答案】B
【解析】
据定义计算反应速率,并利用不同物质表示的反应速率之间的关系进行换算;据可逆反应进行过程中正逆反应速率的变化,比较有关速率的大小;利用Qc与K的关系判断是否化学平衡状态;用平衡移动原理判断平衡移动方向。
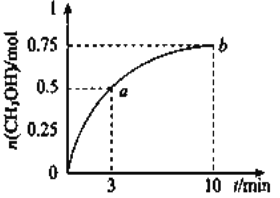
A项:0~10min,n(CH3OH)增加0.75mol,v(CH3OH)=0.75mol/(1L×10min)=0.075mol·L-1·min-1,则v(H2)=0.075mol/(1L×10min)×3=0.225mol·L-1·min-1,A项错误;
B项:据图中数据,点b所在状态有0.25molCO2、1.0molH2、0.75molCH3OH、0.75molH2O(g),将它们的浓度代入Qc表达式,得Qc=2.25=K,为化学平衡状态,B项正确;
C项:从起始到平衡过程中,![]() 的生成速率(正反应速率)逐渐减小,即正反应速率点a高于点b,C项错误;
的生成速率(正反应速率)逐渐减小,即正反应速率点a高于点b,C项错误;
D项:欲使平衡状态时![]() 增大,即使平衡右移。因ΔH<0,可保持其他条件不变降低温度,D项错误。
增大,即使平衡右移。因ΔH<0,可保持其他条件不变降低温度,D项错误。
本题选B。


科目:高中化学 来源: 题型:
【题目】写出化学方程式
(1)硫在氧气中燃烧的化学方程式____
(2)碳粉和氧气的化学反应方程式____
(3)水蒸气与灼热的炭发生氧化还原反应的化学方程式____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚砜(SOCl2)是一种液态化合物,在农药、制药行业中用途广泛。实验室合成原理为:SO2+Cl2+SCl2=2SOCl2,部分装置如图所示,回答以下问题:

已知:①SOCl2沸点为78.8℃,SCl2 的沸点为50℃,且两种液体可互溶。
②SOCl2遇水剧烈反应,液面上产生白雾,并带有刺激性气味的有气体产生。
(1)实验室制取SOCl2在三颈烧瓶中进行,整个装置所选仪器的连接顺序是:⑥→__________→①,②←______________(某些仪器可以多次使用)。
(2)仪器a的名称是________,仪器b的作用是____________。
(3)本实验中制Cl2的离子方程式为___________________,本实验中制SO2的化学方程式为______________________,SOCl2与水反应的化学方程式为___________。
(4)实验结束后,从三颈烧瓶分离出SOCl2的实验操作名称是_________________。若反应中消耗Cl2的体积为896 mL(标准状况,SO2足量),最后得到纯净的SOCl2 7.14 g,则SOCl2的产率为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验:①将![]() 溶液和
溶液和![]() 溶液等体积混合得到浊液;②取少量①中浊液,滴加
溶液等体积混合得到浊液;②取少量①中浊液,滴加![]() 溶液,出现红褐色沉淀;③将①中浊液过滤取少量白色沉淀,滴加
溶液,出现红褐色沉淀;③将①中浊液过滤取少量白色沉淀,滴加![]() 溶液.沉淀变为红褐色。下列说法中,不正确的是 ( )
溶液.沉淀变为红褐色。下列说法中,不正确的是 ( )
A. 将①中浊液过滤,所得滤液中含少量![]()
B. ①中浊液存在平衡:![]()
C. ②中沉淀颜色变化说明![]() 转化为
转化为![]()
D. ③可以证明![]() ,比
,比![]() 更难溶
更难溶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要250 mL 0.5 moL/L的稀硫酸溶液,现用密度为1.84 g/mL,质量分数为98%的浓硫酸配制。请回答下列问题。
(1)下列仪器中,用不到的是__________。
A.250 mL容量瓶 B.500 mL容量瓶 C.50 mL量筒 D.10 mL量筒
(2)若要进行配制,除上述仪器外,尚缺少的仪器或用品是_______________________。
(3) 容量瓶上除有刻线和容量规格外还应标有温度,容量瓶在使用前必须进行的操作是:________。
(4)人们常将配制过程简述如下:①冷却;②洗涤烧杯中的液体;③量取;④溶解;⑤定容;⑥摇匀;⑦移液。其正确的操作顺序是________________________ (填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯是重要的有机化工原料。以丁烯和乙烯为原料反应生成丙烯的方法被称为“烯烃歧化法”,主要反应为![]()
![]()
![]()
已知相关燃烧热数据:
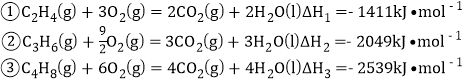
下列说法不正确的是 ( )
A. 消耗等物质的量的原料,反应③的放热最显著
B. 放出相等的热量,反应①产生的![]() 最少
最少
C. “烯烃歧化“反应中消耗![]() ,放热
,放热![]()
D. “烯烃歧化”反应中断键吸收的能量比成键放出的能量多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按指定要求完成下列问题。
(1)在3BrF3+5H2O=HBrO3+Br2+9HF+O2↑的反应中,3mol的BrF3参加反应时,被水还原的BrF3的物质的量是___。
(2)已知砒霜As2O3与Zn可发生如下反应:As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O
①请用双线桥法标出电子转移的方向和数目___。
②若生成0.2molAsH3,则转移的电子数为___。
(3)二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂,制备ClO2有以下两种方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O
①方法一中氧化剂与还原剂的物质的量之比为___。
②若两种方法制备得到相同条件下相同体积的ClO2气体,则两种方法中消耗的还原剂质量之比是___。
③Cl2与ClO2均用作水处理剂,若它们中的氯元素均被还原为Cl-,则相同质量的ClO2是Cl2消毒效率的___倍(消毒效率:等质量两种物质所转移电子的物质的量之比)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在人类文明的历程中,改变世界的事物很多,其中铁、硝酸钾、青霉素、氨、乙醇、二氧化碳、聚乙烯、二氧化硅等17种“分子”改变过人类的世界。
(1)铁原子在基态时,价电子(外围电子)排布式为______________________________。
(2)硝酸钾中![]() 的空间构型为________,写出与
的空间构型为________,写出与![]() 互为等电子体的一种非极性分子化学式__________________________________________________________________。
互为等电子体的一种非极性分子化学式__________________________________________________________________。
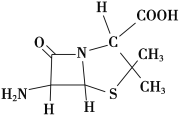
(3)6氨基青霉烷酸的结构如图所示,其中采用sp3杂化的原子有____________。
(4)下列说法正确的有________(填字母序号)。
a.乙醇分子间可形成氢键,导致其沸点比氯乙烷高
b.钨的配合物离子[W(CO)5OH]-能催化固定CO2,该配离子中钨显-1价
c.聚乙烯(CH2CH2)分子中有5n个σ键
d.由下表中数据可确定在反应Si(s)+O2(g)===SiO2(s)中,每生成60 g SiO2放出的能量为(2c-a-b) kJ
化学键 | Si—Si | O===O | Si—O |
键能(kJ·mol-1) | a | b | c |
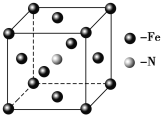
(5)铁和氨气在640 ℃可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式______________________________________。
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是( )
A.铁粉与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑
B.碳酸镁溶于醋酸的反应:MgCO3+2H+=Ca2++CO2↑+H2O
C.在澄清石灰水中通入少量的CO2:Ca2++2OH-+CO2=CaCO3↓+H2O
D.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com